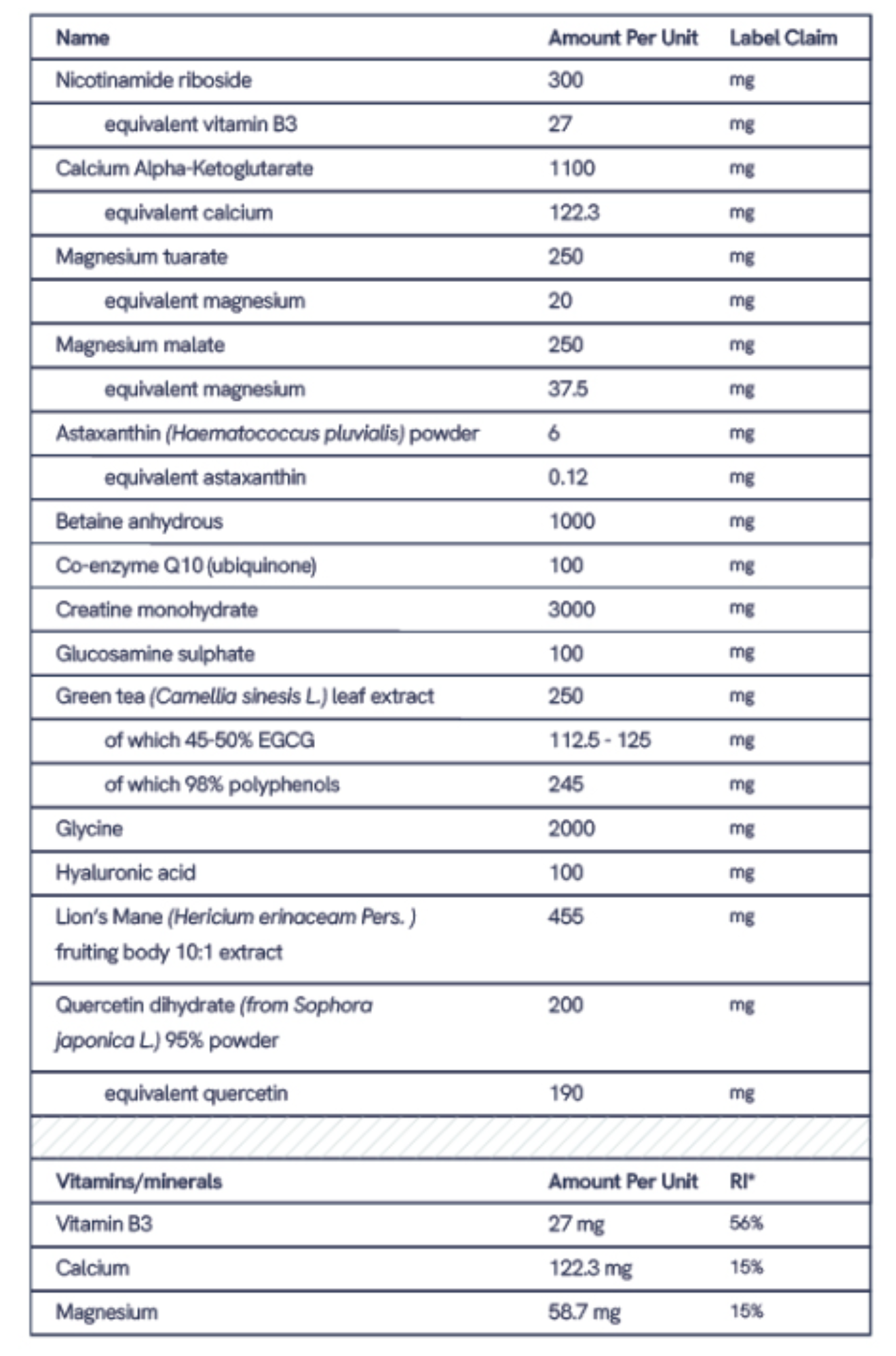
Ein Etikett für Nahrungsergänzungsmittel enthält die Tabelle mit den Nährwertangaben (Wirkstoffe und Dosierungen pro Portion), die Liste der sonstigen Inhaltsstoffe (Füllstoffe, Bindemittel, Überzüge), Allergenwarnungen, Angaben zum Hersteller und etwaige gesundheitsbezogene Angaben. Wenn Sie jeden Abschnitt verstehen, können Sie die Produktqualität bewerten, Rezepturen objektiv vergleichen und Warnzeichen vor dem Kauf erkennen. Das Lesen von Etiketten ist eine der praktischsten Fähigkeiten, die ein Verbraucher von Nahrungsergänzungsmitteln entwickeln kann.
Wichtige Erkenntnisse
- Das Feld „Supplement Facts“ (Nährwertangaben) ist der Abschnitt mit den meisten Informationen auf jedem Etikett: Es enthält Angaben zur Portionsgröße, zu den Inhaltsstoffen, zu den Mengen pro Portion und gegebenenfalls zum prozentualen Anteil des Tagesbedarfs.1
- Bei proprietären Mischungen ist es gesetzlich zulässig, die Namen der Inhaltsstoffe ohne Angabe der einzelnen Mengen aufzulisten, was die Möglichkeit des Verbrauchers einschränkt, die wirksame Dosierung zu beurteilen.1
- Unabhängige Analysen haben ergeben, dass ein erheblicher Teil der Nahrungsergänzungsmittel nicht den Angaben auf dem Etikett entspricht, wobei einige Produkte nicht aufgeführte Inhaltsstoffe enthalten oder deklarierte Inhaltsstoffe fehlen.2
- Zertifizierungsprogramme von Drittanbietern bieten eine unabhängige Überprüfung der Identität der Inhaltsstoffe, ihrer Wirksamkeit und der Abwesenheit von Verunreinigungen – keine dieser Zusicherungen kann allein durch den Aufdruck auf dem Etikett garantiert werden.3
- Von der EFSA genehmigte gesundheitsbezogene Angaben in Europa unterliegen strengen sprachlichen Vorschriften; Ausdrücke wie „trägt bei zu“ oder „unterstützt die normale Funktion“ haben eine definierte rechtliche Bedeutung und werden durch wissenschaftliche Überprüfungen untermauert.
- Ausdrücke wie „heilt“, „beugt vor“ oder „kehrt um“ auf einem Nahrungsergänzungsmittel-Etikett sind nach den europäischen oder US-amerikanischen Rechtsvorschriften nicht zulässig und sollten als Warnsignale behandelt werden.
- Ein Analysezertifikat (COA) eines unabhängigen Labors liefert auf Chargenebene Nachweise darüber, was ein Produkt tatsächlich enthält, unabhängig davon, was auf dem Etikett angegeben ist.
Die Nährwerttabelle entschlüsselt
Das Feld „Supplement Facts“ (Nährwertangaben) ist der regulatorische Kern eines Nahrungsergänzungsmitteletiketts. Zu wissen, wie man es effizient liest, spart Zeit und unterstützt bessere Kaufentscheidungen.
Portionsgröße und Portionen pro Behälter
Die ersten beiden Zeilen jedes Nährwertangabenfeldes geben die Portionsgröße (z. B. „2 Kapseln”) und die Gesamtzahl der Portionen pro Behälter an. Diese beiden Zahlen bestimmen zusammen, wie lange ein Produkt reicht, und ermöglichen eine genaue Berechnung der Kosten pro Dosis. Alle in der Tabelle aufgeführten Inhaltsstoffmengen beziehen sich auf die angegebene Portionsgröße, nicht auf den gesamten Behälter. Wenn auf einem Etikett 500 mg eines bestimmten Inhaltsstoffs angegeben sind, die Portionsgröße jedoch drei Kapseln beträgt und Sie nur eine Kapsel einnehmen, beträgt die tatsächliche Dosis, die Sie erhalten, etwa 167 mg. Diese Unterscheidung ist beim Vergleich von Produkten von erheblicher Bedeutung.1
Nährstoffmengen und Tageswerte
Jeder Inhaltsstoff in der Tabelle ist mit seiner quantitativen Menge pro Portion aufgeführt, ausgedrückt in Milligramm (mg), Mikrogramm (mcg) oder Internationalen Einheiten (IE), je nach Substanz. Neben dieser Menge wird für viele Inhaltsstoffe ein prozentualer Tageswert (%DV) angegeben, der angibt, wie viel der empfohlenen Tagesdosis diese Portion beiträgt. Tageswerte sind von Aufsichtsbehörden festgelegte Referenzwerte für die Bevölkerung und keine personalisierten Empfehlungen. Für viele Inhaltsstoffe, die für die Langlebigkeit relevant sind, wie NAD+-Vorläufer, spezielle Pflanzenstoffe oder neuartige Verbindungen, gibt es keinen festgelegten Tageswert, und in der Spalte %DV wird ein Bindestrich oder ein Sternchen mit einer Fußnote angezeigt, in der die Auslassung erklärt wird. Das Fehlen eines %DV bedeutet nicht, dass ein Inhaltsstoff nicht reguliert ist, sondern lediglich, dass für ihn keine Referenzaufnahme offiziell festgelegt wurde.1
Einheitenumrechnungen: mg, mcg und IU
Eine praktische Quelle für Verwirrung auf den Etiketten von Nahrungsergänzungsmitteln ist die Verwendung unterschiedlicher Maßeinheiten für verschiedene Arten von Inhaltsstoffen. Ein Milligramm (mg) entspricht 1.000 Mikrogramm (mcg). Vitamin D und Vitamin E werden manchmal in Internationalen Einheiten (IE) angegeben, einer Einheit für die biologische Aktivität und nicht einer auf dem Gewicht basierenden Einheit. Zum Vergleich: 1.000 IE Vitamin D3 entsprechen etwa 25 mcg. Beim Vergleich von Produkten gewährleistet die Umrechnung aller Dosierungen in eine gemeinsame Einheit (in der Regel mcg oder mg) aussagekräftige Vergleiche statt oberflächlicher.
Wirkstoffe: Worauf Sie bei Langlebigkeitsformeln achten sollten
Langlebigkeitsorientierte Nahrungsergänzungsmittel gruppieren Inhaltsstoffe oft nach ihrer biologischen Funktion. Das Verständnis dieser Funktionscluster hilft Ihnen zu beurteilen, ob eine Formel logisch aufgebaut ist und ob die enthaltenen Dosierungen mit den bei Menschen untersuchten Dosierungen übereinstimmen.
Energie und Stoffwechselfunktion
B-Vitamine nehmen eine zentrale Position im Energiestoffwechsel ein. Die Vitamine B1 (Thiamin), B3 (Niacin), B6 und B12 tragen zusammen mit Magnesium und Vitamin C zu einem normalen Energiestoffwechsel bei. Sie gehören zu den am häufigsten verwendeten Inhaltsstoffen in Formeln für ein langes Leben und verfügen über fundierte, von der EFSA genehmigte gesundheitsbezogene Angaben. Vitamin B6, B12 und Folsäure tragen zu einem normalen Homocystein-Stoffwechsel bei, einem Stoffwechselweg, der für die Forschung im Bereich der kardiovaskulären und kognitiven Gesundheit relevant ist. Kreatin hat bei einer Einnahme von 3 Gramm pro Tag eine von der EFSA zugelassene Angabe zur Steigerung der körperlichen Leistungsfähigkeit bei aufeinanderfolgenden kurzen, hochintensiven Trainingseinheiten.
Antioxidativer Schutz und Zellfunktion
Vitamin C, Zink und Selen sind die drei Inhaltsstoffe, für die die EFSA Angaben zum Schutz der Zellen vor oxidativem Stress zugelassen hat. Zink trägt außerdem zur normalen DNA-Synthese bei. Diese Inhaltsstoffe sind in vielen Langlebigkeitsprodukten mit mehreren Inhaltsstoffen in Dosierungen enthalten, die die grundlegende antioxidative Funktion unterstützen sollen. Achten Sie bei der Bewertung eines Produkts darauf, dass diese Inhaltsstoffe in Dosierungen enthalten sind, die den in Studien am Menschen verwendeten Mengen entsprechen, und nicht nur in symbolischen Mengen, die für die Kennzeichnung angegeben werden.
Strukturelle und immunologische Unterstützung
Vitamin D, Kalzium, Magnesium und Zink tragen jeweils von der EFSA zugelassene Angaben zum Erhalt normaler Knochen bei. Vitamin D, K und Kalzium sind regelmäßig in Langlebigkeitsformeln enthalten, die auf die Funktion des Bewegungsapparates abzielen. Zur Unterstützung des Immunsystems tragen Vitamin C, D, B6, B12, Folsäure, Zink und Selen jeweils von der EFSA zugelassene Angaben zur normalen Funktion des Immunsystems bei. Eine gut konzipierte Formel enthält diese Stoffe in Mengen, die einen bedeutenden Beitrag zur täglichen Zufuhr leisten, und nicht nur in symbolischen Mengen.
NAD+-Vorläufer und neue Inhaltsstoffe
Einige fortschrittliche Langlebigkeitsformeln enthalten Inhaltsstoffe wie NMN (Nicotinamid-Mononukleotid), NR (Nicotinamid-Ribosid) oder Coenzym Q10. Diese werden in speziellen Artikeln zu den Inhaltsstoffen behandelt. Bei der Bewertung ihrer Aufnahme in eine Kennzeichnung sollten Sie auf die spezifische Form des Inhaltsstoffs (nicht nur auf den Namen der Kategorie), die Dosis pro Portion und darauf achten, ob der Hersteller Verweise auf Studien am Menschen angibt, die diese Dosis belegen. Ohne diese Informationen ist es schwierig zu beurteilen, ob eine angegebene Menge physiologisch sinnvoll ist.
Warnsignale: Proprietäre Mischungen, Füllstoffe und versteckte Dosierungen
Eine der wichtigsten Fähigkeiten beim Lesen von Etiketten auf Nahrungsergänzungsmitteln ist es, Praktiken zu erkennen, die wichtige Informationen darüber verschleiern, was Sie tatsächlich konsumieren.
Proprietäre Mischungen: Was sie sind und warum sie wichtig sind
Eine proprietäre Mischung ist eine Gruppe von Inhaltsstoffen, die unter einem einzigen Sammelnamen auf dem Nährwertkennzeichnungsfeld aufgeführt sind, wobei das Gesamtgewicht der kombinierten Gruppe angegeben wird, ohne jedoch die einzelnen Mengen der einzelnen Inhaltsstoffe offenzulegen. Nach den US-amerikanischen Vorschriften ist dieses Format rechtlich zulässig; es müssen lediglich das Gesamtgewicht der Mischung und die Namen der Inhaltsstoffe innerhalb der Mischung angegeben werden.1 Die europäischen Rahmenbedingungen für Nahrungsergänzungsmittel unterliegen unterschiedlichen Offenlegungspflichten, aber weltweit vermarktete proprietäre Mischungen können den US-amerikanischen Kennzeichnungsvorschriften folgen.
Das Problem für Verbraucher bei proprietären Mischungen ist einfach: Wenn eine Mischung insgesamt 500 mg enthält und zehn Inhaltsstoffe enthält, könnte jeder einzelne Inhaltsstoff 490 mg oder weniger als 1 mg ausmachen, und das Etikett bietet keine Möglichkeit, dies zu bestimmen. Dies ist wichtig, da die wirksamen Dosen der meisten untersuchten Inhaltsstoffe genau definiert sind. Magnesium wird beispielsweise in Studien am Menschen üblicherweise in einer Dosierung von 100 bis 300 mg pro Tag verwendet. Ein Inhaltsstoff, der in einer proprietären Mischung von 200 mg zusammen mit acht anderen Inhaltsstoffen aufgeführt ist, kann einen verschwindend geringen und unwirksamen Anteil ausmachen. Diese Art der Kennzeichnung wird in Verbraucherdiskussionen manchmal als „Pixie-Dusting” bezeichnet: Ein Inhaltsstoff wird in erster Linie aus Gründen der Attraktivität des Etiketts und nicht in einer funktionell relevanten Dosierung hinzugefügt.1
Genauigkeit der Etiketten: Was unabhängige Tests offenbaren
Untersuchungen zum tatsächlichen Inhalt kommerziell verkaufter Nahrungsergänzungsmittel im Vergleich zu den Angaben auf dem Etikett zeigen eine erhebliche Diskrepanz. Eine 2024 in JAMA Network Open veröffentlichte Analyse untersuchte 44 Nahrungsergänzungsmittel zur Gewichtsreduktion und stellte fest, dass 82 % ungenaue Etiketten hatten: 61 % enthielten Inhaltsstoffe, die auf dem Etikett aufgeführt waren, aber analytisch nicht nachgewiesen werden konnten, und 36 % enthielten versteckte Inhaltsstoffe, die nicht auf dem Etikett aufgeführt waren. Keines der Produkte in dieser Studie trug ein Zertifizierungssiegel einer dritten Partei.2 Eine Studie von JAMA Network Open aus dem Jahr 2022, die eine ähnliche Methodik für immununterstützende Nahrungsergänzungsmittel verwendete, identifizierte vergleichbare Muster von Diskrepanzen zwischen Etikett und Inhalt.4 Diese Erkenntnisse stammen aus bestimmten Produktkategorien und lassen sich nicht auf den gesamten Markt für Nahrungsergänzungsmittel übertragen, aber sie unterstreichen, warum der Druck von Etiketten allein als Qualitätssicherungsmechanismus nicht ausreicht.
Gängige Füllstoffe und Hilfsstoffe
Im Abschnitt „Weitere Inhaltsstoffe” auf dem Etikett eines Nahrungsergänzungsmittels sind die nicht aktiven Bestandteile aufgeführt, die bei der Herstellung verwendet werden: Bindemittel, Füllstoffe, Überzüge, Fließmittel und Aromastoffe. Viele davon erfüllen legitime funktionale Aufgaben im Herstellungsprozess. Mikrokristalline Cellulose beispielsweise ist ein häufig verwendeter Füllstoff, der aus pflanzlicher Cellulose gewonnen wird und als unbedenklich gilt. Siliciumdioxid ist ein Fließmittel. Magnesiumstearat ist ein Gleitmittel, das bei der Herstellung von Kapseln und Tabletten verwendet wird. Seine Verwendung in Spurenmengen bei der Herstellung wird aus Sicht der Nahrungsergänzung als unbedeutend angesehen, obwohl dies in der Öffentlichkeit kontrovers diskutiert wird.
Einige Zusatzstoffe werden genauer unter die Lupe genommen. Titandioxid, ein Weißmacher, der in einigen Nahrungsergänzungsmittelbeschichtungen verwendet wird, war Gegenstand einer behördlichen Überprüfung in der Europäischen Union, wo die Europäische Behörde für Lebensmittelsicherheit 2021 zu dem Schluss kam, dass es nicht mehr als sicherer Lebensmittelzusatzstoff angesehen werden kann. Künstliche Farbstoffe und synthetische Süßstoffe in Nahrungsergänzungsmitteln sind ebenfalls erwähnenswert, wenn Sie Formulierungen ohne solche Zusatzstoffe bevorzugen. Wenn Sie den Abschnitt „Weitere Inhaltsstoffe” sorgfältig lesen, können Sie eine fundierte Entscheidung darüber treffen, welche Inhaltsstoffe Sie neben den Wirkstoffen einer Formel gerne zu sich nehmen möchten.
Gesundheitsbezogene Angaben auf Etiketten verstehen
Gesundheitsbezogene Angaben auf den Etiketten von Nahrungsergänzungsmitteln sind nicht alle gleich, und wenn Sie die dahinterstehenden regulatorischen Kategorien verstehen, können Sie besser einschätzen, wie viel Vertrauen in eine bestimmte Aussage eines Produkts über seine Funktion gerechtfertigt ist.
Von der EFSA genehmigte Angaben in Europa
In der Europäischen Union sind gesundheitsbezogene Angaben auf Lebensmitteln und Nahrungsergänzungsmitteln durch die Verordnung (EG) Nr. 1924/2006 geregelt. Die Europäische Behörde für Lebensmittelsicherheit (EFSA) prüft die Angaben anhand wissenschaftlicher Erkenntnisse und genehmigt nur solche, die durch fundierte Daten aus Humanstudien gestützt werden. Genehmigte Angaben folgen einem genau definierten Format. Beispielsweise sind „Magnesium trägt zu einem normalen Energiestoffwechsel bei” und „Vitamin C trägt zu einer normalen Funktion des Immunsystems bei” von der EFSA genehmigte Angaben mit spezifischer rechtlicher Bedeutung. Das Verb „trägt bei” signalisiert in diesem Zusammenhang einen von der EFSA genehmigten Zusammenhang, der durch wissenschaftliche Überprüfungen gestützt wird. Produkte, die auf EU-Märkten verkauft werden und nicht autorisierte oder nicht genehmigte gesundheitsbezogene Angaben tragen, verstoßen gegen die Verordnung und sollten mit Skepsis betrachtet werden.
Achten Sie beim Lesen eines europäischen Nährstoffzusatzetiketts auf Formulierungen, die dem genehmigten Format für Angaben entsprechen. Angaben wie „nachweislich fördert“, „wissenschaftlich erwiesen erhöht“ oder „klinisch nachgewiesen verbessert“ ohne Angabe einer regulatorischen Grundlage sind keine von der EFSA genehmigten Formulierungen. Das Register der EFSA mit genehmigten Angaben ist öffentlich zugänglich und kann verwendet werden, um zu überprüfen, ob eine Angabe auf einem Etikett offiziell bewertet wurde.
Struktur- und Funktionsangaben außerhalb der EFSA
In Märkten außerhalb Europas, einschließlich der Vereinigten Staaten, können die Etiketten von Nahrungsergänzungsmitteln Angaben zu „Struktur und Funktion” enthalten, die keiner Vorabgenehmigung durch eine Aufsichtsbehörde bedürfen. Diese Angaben beschreiben, wie ein Inhaltsstoff die Struktur oder Funktion des Körpers beeinflussen soll, müssen jedoch mit einem Haftungsausschluss versehen sein, der besagt, dass die Angabe nicht von der zuständigen Behörde bewertet wurde und dass das Produkt nicht zur Diagnose, Behandlung, Heilung oder Vorbeugung von Krankheiten bestimmt ist.5 Wenn auf dem Etikett eines Nahrungsergänzungsmittels angegeben ist, dass ein Produkt eine Krankheit „heilt”, „vorbeugt” oder „umkehrt”, ohne dass ein solcher Haftungsausschluss vorhanden ist, entspricht das Etikett nicht den gesetzlichen Anforderungen in den USA und der EU und sollte als ernstzunehmendes Warnsignal betrachtet werden.
Was „verifiziert” und „getestet” auf Etiketten bedeuten
Begriffe wie „im Labor getestet“, „qualitätsgesichert“ und „unter GMP-Bedingungen hergestellt“ beschreiben grundlegende Herstellungsstandards und nicht eine unabhängige Überprüfung auf Produktebene. Die Einhaltung der Guten Herstellungspraxis (GMP) ist eine gesetzliche Vorschrift und kein freiwilliger Qualitätsbonus. Die Zertifizierung durch Dritte umfasst hingegen eine unabhängige Laboranalyse des Endprodukts im Vergleich zu den Angaben auf dem Etikett. In den Konsensleitlinien zu den wesentlichen Merkmalen von Zertifizierungsprogrammen durch Dritte werden die Überprüfung der Etikettengenauigkeit, die Untersuchung auf Verunreinigungen und die Audits der Produktionsstätten als Kernkomponenten einer aussagekräftigen Zertifizierung genannt.3 Ein Analysezertifikat (COA) eines unabhängigen Labors, das auf Anfrage beim Hersteller erhältlich ist, liefert den direktesten Nachweis darüber, was eine bestimmte Charge eines Produkts tatsächlich enthält.
Eine praktische Checkliste zur Bewertung von Etiketten auf Nahrungsergänzungsmitteln
Die folgende Checkliste fasst die wichtigsten Fragen zusammen, die bei der Bewertung eines Nahrungsergänzungsmittels zu stellen sind. Sie dient als Rahmen für einen objektiven Vergleich und ist keine Garantie für Qualität oder Wirksamkeit.
Nährwertangaben: Sind alle Wirkstoffe mit den jeweiligen Mengen pro Portion aufgeführt? Ist die Portionsgröße klar angegeben? Entsprechen die Dosierungen den in der Humanforschung für jeden Inhaltsstoff untersuchten Bereichen?
Proprietäre Mischungen: Sind bestimmte Inhaltsstoffe unter einer Überschrift „proprietäre Mischung” zusammengefasst, ohne dass die einzelnen Mengen angegeben sind? Wenn ja, reicht das Gesamtgewicht der Mischung aus, um alle aufgeführten Inhaltsstoffe in einer sinnvollen Menge bereitzustellen? Kann der Hersteller auf Anfrage die Mengen der einzelnen Inhaltsstoffe angeben?
Sonstige Inhaltsstoffe: Sind die Hilfsstoffe auf solche mit nachgewiesener Sicherheit beschränkt? Sind künstliche Farbstoffe, synthetische Beschichtungen oder Zusatzstoffe, die derzeit einer behördlichen Überprüfung unterliegen, enthalten? Ist die Liste angemessen kurz?
Gesundheitsbezogene Angaben: Entsprechen die Angaben auf dem Etikett den genehmigten behördlichen Formulierungen (EFSA-konforme Formulierungen in Europa)? Werden auf dem Etikett Angaben zu Krankheiten (heilt, beugt vor, kehrt um) vermieden? Gibt es einen angemessenen Haftungsausschluss, wo dies erforderlich ist?
Überprüfung durch Dritte: Trägt das Produkt ein anerkanntes Zertifizierungssiegel einer dritten Partei? Ist ein Analysezertifikat vom Hersteller erhältlich? Veröffentlicht der Hersteller Testdaten?3,6
Herstellerinformationen: Sind der Name und die Kontaktadresse des Herstellers deutlich angegeben? Ist die Qualitätsphilosophie des Unternehmens öffentlich bekannt gegeben und überprüfbar?
Fragen und Antworten
Was ist die Nährwerttabelle?
Das Feld „Supplement Facts“ (Nährwertangaben) ist die vorgeschriebene Nährwertkennzeichnung auf Nahrungsergänzungsmitteln. Es enthält die Portionsgröße, die Anzahl der Portionen pro Behälter, alle Wirkstoffe mit ihrer Menge pro Portion und gegebenenfalls den prozentualen Tagesbedarf. Es ist die wichtigste Informationsquelle darüber, was ein Nahrungsergänzungsmittel enthält und in welcher Dosierung.1
Was ist eine proprietäre Mischung und warum ist sie ein Problem?
Eine proprietäre Mischung ist eine Gruppe von Inhaltsstoffen, die auf dem Etikett eines Nahrungsergänzungsmittels mit ihrem Gesamtgewicht, jedoch ohne Angabe der einzelnen Inhaltsstoffmengen aufgeführt sind. Obwohl dies in einigen Ländern gesetzlich zulässig ist, hindert dieses Format die Verbraucher daran, zu beurteilen, ob ein einzelner Inhaltsstoff in einer Dosis enthalten ist, die mit den untersuchten wirksamen Mengen übereinstimmt. Ohne Kenntnis der einzelnen Dosierungen ist eine aussagekräftige Qualitätsbewertung nicht möglich.1
Was bedeutet „trägt bei zu” auf einem Etikett für Nahrungsergänzungsmittel?
Im regulatorischen Kontext der Europäischen Union ist „trägt bei zu” das Standardverb, das in von der EFSA genehmigten gesundheitsbezogenen Angaben verwendet wird. Es weist darauf hin, dass der Inhaltsstoff wissenschaftlich geprüft und für diese spezifische Angabe gemäß der EU-Verordnung 1924/2006 zugelassen wurde. Es handelt sich um einen rechtlich bedeutsamen Ausdruck und nicht um allgemeine Marketing-Sprache. Aussagen, die eine stärkere oder absolutere Sprache verwenden („bewiesen“, „garantiert“), sind keine von der EFSA zugelassenen Formulierungen.
Was sind die wichtigsten Warnsignale auf einem Etikett für Nahrungsergänzungsmittel?
Zu den wichtigsten Warnsignalen gehören die Verwendung von Krankheitsbehauptungen (das Produkt heilt, verhindert oder kehrt eine bestimmte Erkrankung um), das Fehlen der Dosierungen der einzelnen Inhaltsstoffe in einer proprietären Mischung, das Fehlen einer Zertifizierung durch Dritte, sehr kurze Verfallsdaten und Gesundheitsbehauptungen, die nicht durch eine behördliche Zulassung gestützt werden. Unplausibel umfassende Behauptungen, dass ein einzelnes Produkt alle Bereiche der Gesundheit gleichzeitig unterstützt, ohne dass eine glaubwürdige Formulierungsgrundlage vorliegt, sollten ebenfalls kritisch hinterfragt werden.
Was bedeutet „andere Inhaltsstoffe” auf einem Etikett?
Im Abschnitt „Weitere Inhaltsstoffe” sind die nicht aktiven Bestandteile aufgeführt, die bei der Herstellung des Nahrungsergänzungsmittels verwendet werden, darunter Bindemittel, Füllstoffe, Überzüge, Fließmittel und Aromastoffe. Diese sind keine primären funktionellen Inhaltsstoffe, sondern Teil der physikalischen Struktur des Produkts. Wenn Sie diesen Abschnitt lesen, können Sie Zusatzstoffe identifizieren, die Sie möglicherweise vermeiden möchten, wie z. B. künstliche Farbstoffe oder Überzugsmittel, die in bestimmten Ländern einer behördlichen Überprüfung unterliegen.
Was ist ein Analysezertifikat und wo finde ich es?
Ein Analysezertifikat (COA) ist ein Dokument, das von einem unabhängigen Labor ausgestellt wird und die Ergebnisse der analytischen Prüfung einer bestimmten Charge eines Nahrungsergänzungsmittels bestätigt. Es enthält in der Regel Angaben zur überprüften Identität und Wirksamkeit der Inhaltsstoffe, zum Gehalt an Verunreinigungen (einschließlich Schwermetallen und Keimzahl) und dazu, ob das Produkt den Angaben auf dem Etikett entspricht. Seriöse Hersteller stellen COAs auf ihrer Website oder auf Anfrage zur Verfügung.
Garantiert die „GMP-Zertifizierung” die Produktqualität?
Die Zertifizierung nach den Grundsätzen der guten Herstellungspraxis (GMP) zeigt an, dass eine Produktionsstätte die gesetzlichen Standards für Produktionskonsistenz, Dokumentation, Hygiene und Qualitätskontrolle einhält. Es handelt sich um einen Standard auf Anlagenebene. Er garantiert nicht, dass ein bestimmtes Produkt den Angaben auf dem Etikett entspricht oder frei von Verunreinigungen ist. Unabhängige Produktprüfungen durch Dritte, bei denen das Endprodukt in einem externen Labor analysiert wird, bieten eine direktere Form der Qualitätssicherung.3
Wie rechne ich die Dosierungseinheiten von Nahrungsergänzungsmitteln (mg, mcg, IU) um?
Ein Milligramm (mg) entspricht 1.000 Mikrogramm (mcg). Internationale Einheiten (IE) sind eine biologische Aktivitätseinheit, die für fettlösliche Vitamine verwendet wird. Bei Vitamin D3 entspricht 1 mcg 40 IE (oder 1.000 IE entsprechen 25 mcg). Bei Vitamin E entspricht 1 IE d-alpha-Tocopherol etwa 0,67 mg. Wenn Sie die Dosierungen verschiedener Produkte vergleichen, rechnen Sie alle Werte in die gleiche Einheit um (in der Regel mg oder mcg), um genaue Vergleiche anzustellen.
FAQ
Welche Inhaltsstoffe sind in den Rezepturen der Langlebigkeitspräparate enthalten?
Die Rezepturen der auf Langlebigkeit ausgerichteten Nahrungsergänzungsmittel variieren je nach Produkt, enthalten jedoch in der Regel B-Vitamine (B1, B3, B6, B12, Folsäure), Vitamin C, Vitamin D, Vitamin K, Magnesium, Zink, Selen, Kalzium und oft auch speziellere Inhaltsstoffe wie NAD+-Vorläufer (NMN, NR), Coenzym Q10 oder Kreatin. Eine gut konzipierte Formel gruppiert diese nach ihrer biologischen Funktion: Energiestoffwechsel, antioxidativer Schutz, strukturelle Unterstützung und Zellfunktion. Jeder Inhaltsstoff sollte in einer individuellen Dosierung aufgeführt sein, die im Abschnitt „Nährwertangaben” angegeben ist, und nicht in einer proprietären Mischung versteckt sein.1
Welche Inhaltsstoffe sind in Langlebigkeitsshots enthalten?
Flüssige Langlebigkeits-Shots enthalten in der Regel wasserlösliche Inhaltsstoffe, die in flüssiger Form stabil bleiben, wie B-Vitamine (insbesondere B12 und B6), Vitamin C, Zink und manchmal Pflanzenextrakte oder Aminosäuren. Das Format schränkt die Zugabe von fettlöslichen Vitaminen und Mineralien ein, die in Kapsel- oder Tablettenform mit Nahrungsfett besser bioverfügbar sind. Bei der Bewertung eines Langlebigkeits-Shots gelten die gleichen Grundsätze für das Lesen des Etiketts: Überprüfen Sie, ob die einzelnen Dosierungen aufgeführt sind, ob die gesundheitsbezogenen Angaben den genehmigten behördlichen Formulierungen entsprechen und ob der Hersteller Dokumentationen zu Tests durch Dritte vorlegt.
Was sind die wichtigsten Inhaltsstoffe von Langlebigkeitspräparaten?
Basierend auf der wissenschaftlichen Literatur zu Humanstudien gehören zu den am häufigsten untersuchten Inhaltsstoffen mit Einfluss auf die Langlebigkeit NAD+-Vorläufer (NMN, NR), Kreatin, Coenzym Q10, Omega-3-Fettsäuren, Vitamin D, Magnesium, B-Vitamine und Antioxidantien wie Vitamin C, Zink und Selen. Für eine Reihe dieser Inhaltsstoffe gibt es von der EFSA zugelassene Angaben, die ihre Rolle beim Energiestoffwechsel, der Immunfunktion, dem antioxidativen Schutz und der Erhaltung der Struktur bestätigen. Die Tiefe der wissenschaftlichen Belege variiert je nach Inhaltsstoff. Achten Sie bei der Bewertung von Angaben immer auf Verweise auf von Fachkollegen begutachtete Studien am Menschen.
Welche Inhaltsstoffe sind in Produkten zur Unterstützung der Langlebigkeit enthalten?
Produkte zur Unterstützung der Langlebigkeit basieren in der Regel auf den biologischen Prozessen, die mit gesundem Altern in Verbindung stehen: zelluläre Energieproduktion, Management von oxidativem Stress, Immunregulation und strukturelle Erhaltung von Knochen, Muskeln und Bindegewebe. Zu den häufig enthaltenen Inhaltsstoffen gehören der B-Vitamin-Komplex, Vitamin D, Vitamin K, Magnesium, Zink, Selen und Kalzium, wobei fortgeschrittenere Formeln NAD+-Vorläufer, adaptogene Pflanzenstoffe oder kollagenunterstützende Nährstoffe enthalten. Die Transparenz der Dosierungsangaben, die Verwendung von EFSA-konformen Angaben und die Verfügbarkeit von Testergebnissen unabhängiger Dritte sind die zuverlässigsten Qualitätssignale beim Vergleich dieser Produkte.3
Welche Inhaltsstoffe sind in einer Langlebigkeitsmischung enthalten?
Pulverförmige Langlebigkeitsmischungen enthalten in der Regel wasserlösliche Vitamine, Mineralien und manchmal Aromastoffe oder natürliche Süßungsmittel, die die Schmackhaftigkeit in flüssiger Form unterstützen. Eine umfassende Langlebigkeitsmischung kann Vitamin C, B-Vitamine, Magnesium, Zink, Kreatin und in einigen Fällen NAD+-Vorläufer oder Kollagenpeptide enthalten. Bei der Pulverform muss der Hersteller die Stabilität der Inhaltsstoffe in Wasser berücksichtigen. Wie bei jeder Form von Nahrungsergänzungsmitteln ist die Angabe der einzelnen Dosierungen anstelle von proprietären Mischungen der wichtigste Indikator für die Transparenz, der bewertet werden muss.1
Wie kann ich überprüfen, ob eine gesundheitsbezogene Angabe zu einem Nahrungsergänzungsmittel legitim ist?
In Europa ist das Register der EFSA für zugelassene nährwert- und gesundheitsbezogene Angaben unter ec.europa.eu/food/safety/labelling_nutrition/claims öffentlich zugänglich. Sie können nach beliebigen Inhaltsstoffen suchen und sehen, welche Angaben genehmigt, abgelehnt oder noch ausstehend sind. Bei genehmigten Angaben wird der genaue zulässige Wortlaut angegeben. Wenn eine Angabe auf einem Produktetikett nicht mit dem genehmigten Wortlaut übereinstimmt, ist sie entweder nicht genehmigt oder eine Umschreibung, die möglicherweise nicht die gleiche rechtliche Grundlage hat. Im Allgemeinen sind Angaben, die die Vorbeugung, Behandlung oder Heilung von Krankheiten versprechen, weder in der EU noch in den USA auf Etiketten von Nahrungsergänzungsmitteln gesetzlich zulässig und stellen ein deutliches Warnsignal dar.
- Saldanha LG, Dwyer JT, Haggans CJ, Mills JL, Dunlop RH. Perspektiven zur Verwendung proprietärer Mischungen in Nahrungsergänzungsmitteln. Aktuelle Entwicklungen in der Ernährung. 2023;7(5):100071. Auf PubMed anzeigen ↗
- Crawford C, Avula B, Lindsey AT, Katragunta K, Khan IA, Deuster PA. Genauigkeit und Qualität der Etiketten ausgewählter Nahrungsergänzungsmittel zur Gewichtsreduktion, die auf oder in der Nähe von US-Militärstützpunkten verkauft werden. JAMA Network Open. 2024;7(5):e249131. Anzeigen auf PubMed ↗
- Antonio J, Burd N, Ellerbroek A, et al. Wesentliche Merkmale von Zertifizierungsprogrammen für Nahrungsergänzungsmittel durch Dritte: Eine Konsenserklärung. Zeitschrift der Internationalen Gesellschaft für Sporternährung. 2019;16(1):33. Anzeigen auf PubMed ↗
- Crawford C, Avula B, Lindsey AT, Walter A, Katragunta K, Khan IA, Deuster PA. Analyse ausgewählter Nahrungsergänzungsmittel, die zur Unterstützung oder Stärkung des Immunsystems vermarktet werden. JAMA Network Open. 2022;5(8):e2226040. Anzeigen auf PubMed ↗
- Parrish RS, Lansberg PJ, Skokan LN. Narrative Review: Der oberflächliche Ansatz der FDA bei der Regulierung von Nahrungsergänzungsmitteln führt zu zahlreichen Berichten über unerwünschte Ereignisse. Open Access Emergency Medicine. 2023;15:415–424. Anzeigen auf PubMed ↗
- Hathcock J. Datenqualität und Transparenz in der Nahrungsergänzungsmittelindustrie. Regulatory Toxicology and Pharmacology. 2014;68(3):273–274. Auf PubMed anzeigen ↗