L'hormèse est un phénomène biologique dans lequel une exposition brève et à faible dose à un facteur de stress déclenche des réponses adaptatives qui renforcent l'organisme. L'exposition au froid, le sauna, le jeûne et l'exercice physique activent tous les voies hormétiques, notamment la libération de noradrénaline, l'induction des protéines de choc thermique, l'activation de l'AMPK et la signalisation des sirtuines. Le facteur critique est la relation dose-réponse : une dose trop faible n'a aucun effet, une dose adéquate génère une adaptation et une dose trop élevée cause des dommages.
Points clés à retenir
- L'hormèse suit une courbe dose-réponse en forme de U inversé : un petit facteur de stress stimule une adaptation bénéfique, tandis qu'une exposition excessive produit des dommages.1
- L'immersion dans l'eau froide active le système nerveux sympathique. Des études menées sur des humains ont montré une augmentation de plus de 500 % du taux de noradrénaline plasmatique par rapport aux niveaux au repos.2
- Dans une cohorte prospective finlandaise de plus de 2 000 hommes, une utilisation plus fréquente du sauna a été associée à un risque nettement plus faible d'événements cardiovasculaires mortels par rapport à une utilisation hebdomadaire.3
- Une séance intense d'exercices par intervalles à haute intensité chez l'être humain active l'AMPK et la p38 MAPK dans les muscles squelettiques et augmente l'expression du PGC-1alpha, signalant la biogenèse mitochondriale.4
- Le jeûne intermittent active l'autophagie via la signalisation AMPK-mTOR et augmente l'activité des sirtuines, deux voies associées à l'entretien cellulaire et à la longévité.5
- La relation dose-réponse hormétique est très conservée dans les systèmes biologiques et est pertinente pour comprendre les limites de la plasticité adaptative chez l'être humain.8
Chapitre 1 : Le concept d'hormèse — Comment le stress devient une force
L'expression « ce qui ne te tue pas te rend plus fort » est plus qu'un proverbe. Elle reflète un mécanisme biologique spécifique que les chercheurs étudient depuis plus d'un siècle sous le terme d'hormèse.
L'hormèse décrit une relation dose-réponse biphasique dans laquelle une faible dose d'un facteur de stress produit un effet stimulant ou bénéfique, tandis qu'une dose élevée du même facteur de stress produit un effet inhibiteur ou nocif.1 Lorsqu'on les représente graphiquement, on obtient une courbe en U inversé caractéristique : une zone à faible dose où les performances biologiques s'améliorent, un pic, puis une zone à forte dose où les performances diminuent ou où les dommages s'accumulent.
Ce concept trouve ses racines dans les travaux du médecin du XVIe siècle Paracelse, qui a remarqué que la différence entre un médicament et un poison réside souvent dans la dose. Le cadre scientifique moderne de l'hormèse a été développé en grande partie grâce aux travaux de toxicologues et de biogérontologues à la fin du XXe siècle, qui ont reconnu que ce phénomène n'était pas une exception, mais une règle dans tous les systèmes biologiques.1
Ce qui rend l'hormèse particulièrement pertinente pour la longévité, c'est l'observation que bon nombre des réponses adaptatives déclenchées par des facteurs de stress légers (production de protéines de choc thermique, activation d'enzymes de réparation, stimulation de l'autophagie) sont les mêmes processus qui déclinent avec le vieillissement. Les chercheurs ont émis l'hypothèse que la capacité à déclencher une réponse hormétique robuste pourrait elle-même définir les limites de la plasticité biologique et, en fin de compte, de la longévité.8
Quatre facteurs de stress pratiques sont particulièrement pertinents pour les personnes intéressées par la longévité : l'exposition délibérée au froid, l'exposition délibérée à la chaleur, l'exercice physique et le jeûne périodique. Chacun d'entre eux active des voies hormétiques qui se recoupent mais qui sont distinctes, et les preuves scientifiques à leur sujet chez l'homme sont de plus en plus nombreuses.
Chapitre 2 : Hormèse froide — Noradrénaline, graisse brune et adaptation cellulaire
L'immersion dans l'eau froide et les douches froides représentent certaines des plus anciennes pratiques hormétiques délibérées de l'histoire. D'un point de vue physiologique, une brève exposition au froid est un facteur de stress contrôlé qui active le système nerveux sympathique, induisant une cascade de réponses adaptatives.
La réponse la plus immédiate et la mieux documentée est une forte augmentation de la noradrénaline plasmatique. Dans une étude contrôlée menée sur des hommes en bonne santé immergés dans de l'eau à 14 °C, les chercheurs ont rapporté une augmentation d'environ 530 % des concentrations plasmatiques de noradrénaline par rapport aux niveaux au repos, et une augmentation d'environ 250 % de la dopamine.2 Cette activation sympathique est considérée comme l'un des principaux facteurs responsables des effets aigus du rhume sur la vigilance et l'humeur.
Au-delà de la réponse neurochimique immédiate, l'exposition répétée au froid est associée à des changements adaptatifs dans la façon dont le corps régule la température et le taux métabolique. Le tissu adipeux brun, un dépôt de graisse spécialisé qui génère de la chaleur en brûlant des calories, est connu pour être activé par le froid et pour augmenter de volume lors d'une exposition répétée au froid chez l'être humain. L'activation de ce tissu représente une véritable adaptation métabolique, et non une simple réponse aiguë à l'inconfort.
Au niveau cellulaire, l'exposition au froid a été étudiée pour son association avec l'expression de protéines induites par le froid et d'éléments de réponse au stress. Le point central du point de vue de l'hormèse est la dépendance à la dose : des expositions brèves et répétées à une intensité qui génère une réponse au stress significative mais tolérable sont considérées comme plus bénéfiques qu'une exposition minimale ou un froid extrême prolongé. L'objectif est le stimulus adaptatif, et non la dose maximale supportable.
D'un point de vue pratique, les protocoles d'immersion dans l'eau froide étudiés dans le cadre de recherches impliquent généralement des températures de l'eau comprises entre 10 et 20 degrés Celsius et des durées d'une à dix minutes. Les variations individuelles en matière de tolérance au froid sont importantes, et toute personne envisageant une exposition délibérée au froid doit le faire progressivement et en tenant compte des contre-indications, notamment les troubles cardiovasculaires.
Chapitre 3 : Hormèse thermique — Protéines de choc thermique et adaptation cardiovasculaire
L'exposition à la chaleur, en particulier par l'utilisation traditionnelle du sauna, fait partie des pratiques hormétiques les plus étudiées chez l'homme. Les données de la cohorte finlandaise, en particulier, ont produit certaines des preuves observationnelles les plus convaincantes établissant un lien entre un facteur de stress thermique délibéré et des résultats associés à la longévité.
Dans une étude de cohorte prospective portant sur 2 315 hommes finlandais d'âge moyen suivis pendant 20 ans, Laukkanen et ses collègues ont examiné la relation entre la fréquence des séances de sauna et la mortalité. Par rapport aux hommes qui utilisaient le sauna une fois par semaine, ceux qui l'utilisaient quatre à sept fois par semaine présentaient des taux nettement inférieurs d'événements cardiovasculaires mortels et de mortalité toutes causes confondues, avec des associations qui persistaient après ajustement pour les facteurs de risque cardiovasculaires conventionnels, l'activité physique et le statut socio-économique.3 Ces conclusions ont ensuite été étendues aux femmes dans une analyse distincte, qui a fait état d'associations directionnelles similaires.7
Ces conclusions doivent être considérées avec prudence. Les études de cohorte observationnelles ne permettent pas d'établir un lien de causalité, et les facteurs de confusion, notamment les comportements sains qui coïncident avec l'utilisation régulière du sauna, ne peuvent être totalement exclus. Les données existantes représentent des associations plutôt que des avantages causaux prouvés.
Le mécanisme biologique proposé par lequel l'exposition à la chaleur peut produire des avantages adaptatifs est centré sur les protéines de choc thermique, en particulier les HSP70 et HSP90. Ces chaperons moléculaires sont induits par le stress cellulaire lié à des températures élevées et jouent un rôle dans la protection des protéines contre les mauvais repliements, la facilitation de la réparation cellulaire et le soutien de la régulation immunitaire. L'induction des protéines de choc thermique représente une réponse hormétique : le stress thermique modéré d'une séance de sauna est suffisant pour stimuler l'expression des protéines protectrices sans causer de dommages tissulaires.
D'autres réactions physiologiques à l'exposition à la chaleur ont été documentées dans des études humaines, notamment une augmentation transitoire du rythme cardiaque, une amélioration de la compliance artérielle et une augmentation du volume plasmatique. Ces adaptations cardiovasculaires ressemblent, à certains égards, aux effets d'un exercice aérobique modéré, ce qui a conduit les chercheurs à décrire l'utilisation du sauna comme une forme de conditionnement cardiovasculaire passif.
Dans la tradition finlandaise, la température des saunas varie généralement entre 80 et 100 degrés Celsius avec un faible taux d'humidité, et les séances durent entre 10 et 20 minutes. Comme pour l'exposition au froid, la réaction individuelle varie et l'exposition à la chaleur est contre-indiquée chez certaines populations cliniques. Toute personne souffrant d'une maladie cardiovasculaire ou d'autres problèmes de santé importants doit consulter un professionnel de santé qualifié avant de commencer à pratiquer régulièrement le sauna.
Chapitre 4 : L'hormèse de l'exercice — Du stress mitochondrial à l'activation de l'AMPK
L'exercice physique est peut-être le facteur de stress hormétique le plus étudié. Chaque effort physique impose un stress contrôlé à l'organisme (augmentation des espèces réactives de l'oxygène, épuisement des réserves de glycogène, génération de sous-produits métaboliques) et l'organisme réagit en développant sa capacité d'adaptation. Au fil du temps, il en résulte un organisme plus fort et plus efficace sur le plan métabolique.
Au niveau cellulaire, l'exercice active deux des protéines de signalisation les plus importantes dans la science de la longévité : l'AMPK (protéine kinase activée par l'AMP) et la PGC-1alpha (coactivateur 1-alpha du récepteur gamma activé par les proliférateurs de peroxysomes).
Dans une étude sur la biopsie musculaire humaine, Gibala et ses collègues ont découvert qu'une séance intense d'exercices par intervalles à haute intensité augmentait considérablement la phosphorylation de l'AMPK et l'activation de la p38 MAPK dans le muscle vaste latéral humain, l'ARNm du PGC-1alpha augmentant d'environ deux fois par rapport aux niveaux de repos pendant la récupération.4 Cette signature moléculaire est associée au déclenchement de la biogenèse mitochondriale, processus par lequel les cellules construisent de nouvelles mitochondries afin d'augmenter leur capacité de production d'énergie.
L'AMPK fonctionne comme un capteur d'énergie cellulaire. Lorsque le rapport AMP/ATP augmente, comme c'est le cas lors d'un exercice intense, d'un jeûne ou de périodes de stress énergétique, l'AMPK est activée. Une fois active, l'AMPK favorise les processus cataboliques (absorption du glucose, oxydation des graisses, biogenèse mitochondriale) et inhibe les processus anaboliques (croissance cellulaire, synthèse des protéines via mTOR). Ce changement métabolique est l'un des mécanismes centraux qui relient l'exercice physique à l'entretien cellulaire associé à la longévité.
Deux modalités d'exercice semblent activer des voies hormétiques partiellement distinctes. L'entraînement en zone 2, caractérisé par un effort constant à une intensité faible à modérée, est associé à une activation soutenue de l'AMPK et à une biogenèse mitochondriale robuste au fil du temps. L'entraînement par intervalles à haute intensité produit une activation plus nette et plus aiguë de l'AMPK et de la p38 MAPK par unité de temps, ainsi que la libération de myokines, des molécules de signalisation sécrétées par les muscles en contraction qui influencent d'autres tissus, notamment le cerveau, le foie et le tissu adipeux. Un programme d'exercice bien conçu dans un but de longévité peut tirer profit de l'intégration des deux modalités.
Le principe de l'hormèse s'applique clairement ici : trop peu d'exercice ne produit aucun stimulus adaptatif significatif, la bonne dose produit une adaptation, et un entraînement excessif sans récupération adéquate conduit au syndrome de surentraînement, à une suppression immunitaire et à un risque accru de blessures. La récupération n'est pas l'absence d'entraînement, c'est le moment où la réponse adaptative est consolidée.
Chapitre 5 : Hormèse du jeûne — Autophagie, activation des sirtuines et nettoyage cellulaire
Le jeûne périodique est l'un des facteurs de stress hormétiques les plus puissants dont dispose l'être humain. Lorsque le corps est privé d'apport calorique pendant une période suffisante, il réagit en activant une série de mécanismes de survie qui privilégient l'entretien et la réparation cellulaires plutôt que la croissance et la reproduction.
Deux des événements moléculaires les plus importants déclenchés par le jeûne sont l'induction de l'autophagie et l'activation des sirtuines.
L'autophagie, du grec « auto-alimentation », est le processus cellulaire par lequel les protéines endommagées, les organites dysfonctionnels et autres débris cellulaires sont décomposés et recyclés. Elle représente un mécanisme de contrôle de la qualité essentiel à la longévité cellulaire et qui est altéré avec le vieillissement. Le jeûne active l'autophagie par le biais de l'axe AMPK-mTOR : lorsque l'apport calorique diminue, l'AMPK est activée et la mTOR (cible mécanistique de la rapamycine) est inhibée. Comme la mTOR supprime normalement l'autophagie, son inhibition permet au programme d'autophagie de se dérouler.5
Les sirtuines sont une famille d'enzymes désacétylases qui régulent un large éventail de processus biologiques, notamment la réparation de l'ADN, l'inflammation et l'adaptation métabolique. L'activité des sirtuines dépend de la disponibilité du NAD+, dont les niveaux augmentent pendant le jeûne lorsque la cellule passe à l'oxydation des acides gras. De cette manière, le jeûne relie directement l'état énergétique de la cellule à sa capacité d'entretien et de réparation.6
Une étude exhaustive menée par de Cabo et Mattson dans le New England Journal of Medicine a résumé les preuves suggérant que le jeûne intermittent, y compris les protocoles d'alimentation à durée limitée et de jeûne un jour sur deux, active ces voies adaptatives conservées chez l'homme et est associé à une série d'améliorations métaboliques, notamment une meilleure sensibilité à l'insuline, une réduction des marqueurs inflammatoires et une meilleure résistance au stress.5 Les examinateurs ont toutefois noté que la traduction des résultats obtenus à partir de modèles animaux et d'essais cliniques à court terme sur des humains en recommandations cliniques définitives à long terme nécessite des études supplémentaires.
Le principe de l'hormèse s'applique au jeûne comme à tous les facteurs de stress. Des périodes de jeûne occasionnelles de 12 à 24 heures sont conformes aux schémas selon lesquels les humains ont évolué et sont bien tolérées par la plupart des adultes en bonne santé. Un jeûne prolongé au-delà de cette durée comporte un profil de risque différent et n'entre pas dans le cadre de cette présentation éducative. Les personnes ayant des antécédents de troubles alimentaires, de diabète ou d'autres problèmes de santé pertinents ne doivent pas suivre de protocoles de jeûne sans surveillance médicale.
Chapitre 6 : Le principe dose-réponse — Comment l'hormèse échoue lorsque la dose est incorrecte
La compréhension de l'hormèse n'est pas complète sans la compréhension de ses limites. La courbe en U inversé signifie que la même intervention qui est bénéfique à dose modérée peut être neutre à faible dose et nocive à forte dose.
Dans le contexte de l'exercice physique, ce mode de défaillance est le syndrome de surentraînement, un état dans lequel le stress cumulé de l'exercice sans récupération adéquate supprime la fonction immunitaire, augmente le risque de blessure, élève le cortisol au repos et peut accélérer plutôt que ralentir les marqueurs biologiques du vieillissement. La réponse adaptative ne se produit que pendant la période de récupération, et non pendant le stress lui-même.
Dans le contexte de la chaleur et du froid, les modes de défaillance sont respectivement l'hyperthermie et l'hypothermie, des extrêmes qui causent des dommages physiologiques plutôt que l'adaptation.
Dans le contexte du jeûne, une restriction calorique sévère prolongée peut entraîner une perte musculaire, des perturbations hormonales et des carences nutritionnelles lorsqu'elle est pratiquée sans surveillance adéquate.
Une découverte issue de la recherche sur l'hormèse qui a un lien direct avec l'utilisation des compléments alimentaires est le paradoxe antioxydant. Certaines études ont montré que la prise de compléments antioxydants à forte dose immédiatement après l'exercice atténue la signalisation adaptative associée à l'exercice, potentiellement parce que les espèces réactives de l'oxygène produites pendant l'exercice servent de signal hormétique initial pour l'activation de l'AMPK et la biogenèse mitochondriale. Cela ne signifie pas que les antioxydants sont nocifs — ils sont bénéfiques dans des contextes appropriés — mais cela illustre que les réponses adaptatives du corps au stress sont finement calibrées et peuvent être perturbées par un signal trop intense.
Le principe pratique issu de la recherche sur l'hormèse est le suivant : rechercher la dose qui produit une réponse au stress significative mais récupérable, permettre une récupération adéquate et répéter. La cohérence et un dosage approprié favorisent l'adaptation. Une intensité extrême sans récupération ne le fait pas.
Chapitre 7 : Compléments alimentaires qui interagissent avec les voies hormétiques
Plusieurs compléments alimentaires ont été étudiés pour leur potentiel à soutenir les voies cellulaires activées par les facteurs de stress hormétiques. Cette section les présente uniquement dans un contexte éducatif. Aucune allégation relative aux compléments alimentaires ne va au-delà de ce qui est actuellement étayé par des preuves humaines et les cadres réglementaires.
Le magnésium intervient dans plus de 300 réactions enzymatiques et joue un rôle dans le métabolisme énergétique, la fonction musculaire et la synthèse des protéines. Le magnésium contribue au métabolisme énergétique normal et aide à réduire la fatigue et l'épuisement, deux allégations de santé approuvées par l'EFSA et pertinentes pour la récupération après un effort physique. La supplémentation en magnésium pour maintenir un niveau adéquat, en particulier chez les personnes très actives physiquement, est une stratégie nutritionnelle raisonnable.
La créatine augmente les performances physiques lors d'efforts successifs de courte durée et de haute intensité, et améliore la force musculaire chez les adultes de plus de 55 ans qui pratiquent régulièrement des exercices de résistance — deux allégations approuvées par l'EFSA. La créatine est donc directement liée à l'hormèse de l'exercice physique, car elle répond aux exigences de performance aiguës des entraînements par intervalles à haute intensité et des exercices de résistance.
Le resvératrol et les polyphénols apparentés ont été étudiés en tant que composés xénohormétiques potentiels, c'est-à-dire des molécules alimentaires susceptibles d'activer certaines des voies de réponse au stress identiques à celles activées par les facteurs de stress physiques, notamment l'activation des sirtuines. Les preuves de ces effets chez l'homme restent préliminaires et doivent être interprétées avec prudence.
Le NMN et le NR, précurseurs du NAD+, sont étudiés pour leur potentiel à soutenir les fonctions NAD+-dépendantes des sirtuines, qui sont activées par l'hormèse du jeûne. Des essais sur l'homme sont en cours, et les allégations concernant des résultats spécifiques ne doivent pas aller au-delà de ce que les preuves actuelles permettent de soutenir.
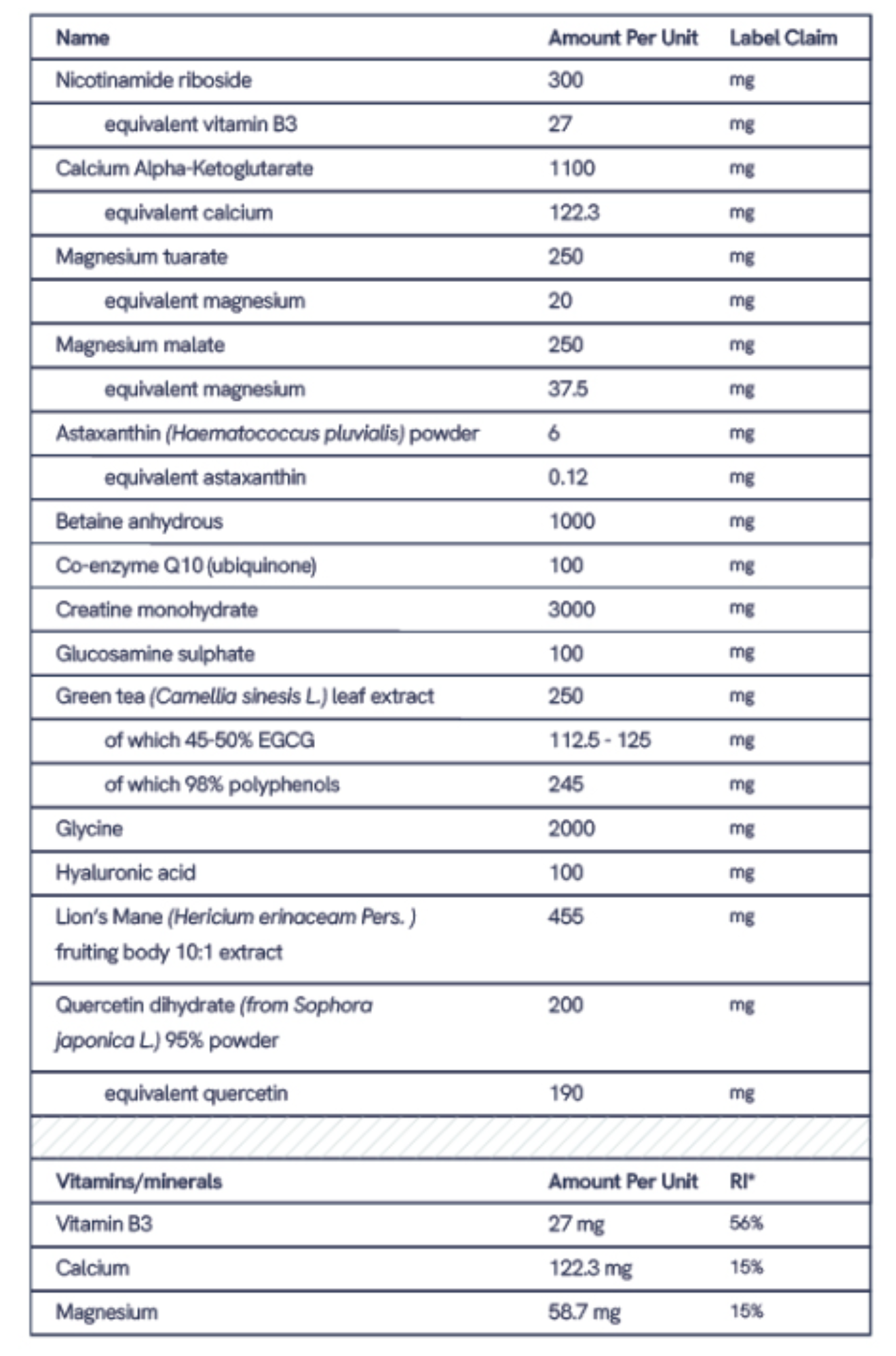
Longevity Complete de The Longevity Store est formulé pour inclure du magnésium, de la créatine, des vitamines B, de la vitamine C, du zinc et d'autres nutriments dont l'efficacité a été prouvée. Il a été testé de manière indépendante par le laboratoire Eurofins et détient la certification NZVT « sans dopage ». Lorsque cela est pertinent pour soutenir le métabolisme énergétique normal, la fonction musculaire et la récupération, ses ingrédients sont formulés à des doses étudiées.
Questions-réponses
Que signifie réellement le mot « hormèse » ?
Le terme « hormèse » vient du grec et signifie « mettre en mouvement » ou « stimuler ». En biologie, il décrit un phénomène de relation dose-réponse dans lequel une faible dose d'un facteur de stress produit un effet stimulant bénéfique, tandis qu'une dose élevée du même facteur de stress produit un effet inhibiteur ou nocif.1 C'est la base scientifique de l'observation selon laquelle de petites quantités de stress physique ou physiologique peuvent renforcer plutôt qu'affaiblir les systèmes biologiques.
Pourquoi l'exposition au froid semble-t-elle améliorer l'humeur et l'énergie ?
L'immersion dans l'eau froide active le système nerveux sympathique, provoquant une libération importante de noradrénaline. Des études menées sur des humains ont montré une augmentation de plus de 500 % du taux de noradrénaline plasmatique pendant l'immersion dans l'eau froide par rapport aux niveaux au repos.2 La noradrénaline est associée à la vigilance, à l'attention et à un effet positif. Cette réponse neurochimique aiguë est l'un des facteurs susceptibles de contribuer à l'amélioration de l'humeur et de l'énergie que de nombreuses personnes rapportent après une exposition au froid.
Existe-t-il des preuves scientifiques de l'effet bénéfique du sauna sur la longévité ?
Oui, bien que les preuves soient observationnelles plutôt que issues d'essais contrôlés randomisés. Une étude de cohorte prospective finlandaise a révélé que les hommes qui utilisaient le sauna quatre à sept fois par semaine présentaient des taux d'événements cardiovasculaires mortels nettement inférieurs à ceux qui l'utilisaient une fois par semaine, après ajustement des facteurs de risque cardiovasculaire connus.3 Des recherches ultérieures ont étendu ces conclusions aux femmes.7 Ces études ne peuvent prouver la causalité, mais les données sont cohérentes et le mécanisme biologique (induction des protéines de choc thermique et conditionnement cardiovasculaire) est plausible.
Que se passe-t-il dans les cellules musculaires pendant l'exercice au niveau moléculaire ?
Pendant un exercice intense, les besoins énergétiques des muscles en contraction entraînent une augmentation du rapport AMP/ATP. Cela active l'AMPK, qui à son tour stimule le PGC-1alpha, un régulateur principal de la biogenèse mitochondriale. Des études de biopsie musculaire humaine ont confirmé que même une brève séance d'exercice par intervalles à haute intensité suffit pour activer la signalisation AMPK et p38 MAPK et augmenter l'expression du gène PGC-1alpha en quelques heures.4 Au fil des séances répétées, cela conduit à une augmentation de la densité mitochondriale et de la capacité aérobie.
Comment le jeûne déclenche-t-il l'autophagie ?
Pendant le jeûne, l'épuisement du glucose et des acides aminés réduit l'activité du mTOR, le capteur de croissance cellulaire qui supprime normalement l'autophagie. Simultanément, l'AMPK est activée par la chute de l'ATP cellulaire. Ces deux changements combinés déclenchent le programme d'autophagie, permettant aux cellules de décomposer et de recycler les protéines et les organites endommagés. Ce processus est considéré comme un mécanisme important de maintenance cellulaire qui décline avec le vieillissement.5
Les quatre facteurs de stress hormétiques (le froid, la chaleur, l'exercice physique et le jeûne) agissent-ils tous de la même manière ?
Ils partagent certains nœuds de signalisation communs, en particulier l'activation de l'AMPK, mais chaque facteur de stress active également des voies distinctes. Le froid sollicite principalement le système nerveux sympathique et les protéines de choc froid. La chaleur induit principalement les protéines de choc thermique et les adaptations cardiovasculaires. L'exercice active l'AMPK, la p38 MAPK et la sécrétion de myokines. Le jeûne active la signalisation AMPK-mTOR, l'activité des sirtuines et la production de corps cétoniques. Ce chevauchement suggère qu'une synergie est possible lorsque les facteurs de stress sont combinés intelligemment avec une récupération adéquate, bien que les preuves formelles d'une combinaison optimale chez l'homme restent limitées.6
Peut-on faire trop d'hormèse ?
Oui. La relation dose-réponse en U inversé signifie que tous les facteurs de stress hormétiques ont une limite supérieure au-delà de laquelle ils deviennent nocifs. Le syndrome de surentraînement, l'hyperthermie, l'hypothermie et la restriction calorique sévère représentent les modes de défaillance lorsque les facteurs de stress hormétiques sont appliqués à une intensité excessive ou sans récupération adéquate. L'objectif est d'identifier la dose qui produit une réponse adaptative significative, et non la dose maximale tolérable.1
Dois-je prendre des compléments antioxydants les jours où je fais de l'exercice ?
Il s'agit d'un domaine où les preuves suggèrent la prudence quant au moment choisi. Certaines recherches indiquent que la prise de compléments antioxydants à forte dose immédiatement après l'exercice peut atténuer les espèces réactives de l'oxygène qui servent de signal hormétique initial pour l'activation de l'AMPK et l'adaptation mitochondriale. Cela ne signifie pas que les nutriments antioxydants sont globalement nocifs — le zinc, la vitamine C et le sélénium jouent un rôle important dans la protection cellulaire normale — mais le moment choisi par rapport à l'exercice peut avoir son importance. Il est conseillé de consulter un professionnel de santé qualifié au sujet de votre protocole de compléments spécifique.
FAQ
Qu'est-ce que l'hormèse en termes simples ?
L'hormèse est le principe biologique selon lequel de petites doses d'un facteur de stress peuvent renforcer l'organisme. L'eau froide, la chaleur, l'exercice physique et le jeûne en sont des exemples concrets : chacun d'entre eux crée un stress contrôlé qui incite l'organisme à s'adapter et à devenir plus résistant au fil du temps. La clé réside dans la dose : une dose trop faible n'apporte aucun bénéfice, une dose adéquate entraîne une adaptation, tandis qu'une dose trop importante est nocive.1
L'hormèse est-elle synonyme de stress ?
L'hormèse est un type spécifique de réponse bénéfique au stress. Tous les stress ne sont pas hormétiques : le stress psychologique chronique, par exemple, ne produit pas les mêmes avantages adaptatifs que les facteurs de stress physique brefs. Le stress hormétique se caractérise par une durée brève, une intensité contrôlée et un temps de récupération adéquat, ce qui permet au corps de mettre en place une réponse adaptative plutôt que d'être chroniquement épuisé.
Quel est le lien entre l'hormèse due à l'exercice physique et la longévité ?
L'exercice physique active l'AMPK et la PGC-1alpha dans les muscles squelettiques humains, stimulant la biogenèse mitochondriale et améliorant l'efficacité métabolique.4 Ces adaptations sont associées à une amélioration des marqueurs de la durée de vie en bonne santé, notamment la capacité aérobie, la sensibilité à l'insuline et l'équilibre inflammatoire. Le principe hormétique explique pourquoi une activité physique d'intensité modérée pratiquée régulièrement est plus bénéfique pour la longévité que l'absence d'activité physique ou un entraînement extrême sans récupération.
Le jeûne intermittent peut-il favoriser l'hormèse ?
Oui. Le jeûne périodique active la voie AMPK-mTOR, stimulant l'autophagie et l'activité des sirtuines, des processus de maintenance cellulaire associés à la recherche sur la longévité. Une étude publiée dans le New England Journal of Medicine a conclu que le jeûne intermittent active ces voies chez l'homme et est associé à des améliorations métaboliques, bien que les auteurs aient noté que les recommandations cliniques à long terme nécessitent des études supplémentaires.5
L'utilisation du sauna est-elle une forme d'hormèse ?
L'utilisation du sauna est considérée comme une pratique d'hormèse thermique. Elle induit l'expression de protéines de choc thermique, une adaptation cardiovasculaire et des réponses inflammatoires transitoires chez l'être humain. Des données observationnelles de cohorte provenant de Finlande associent l'utilisation régulière du sauna à une mortalité cardiovasculaire plus faible, bien que cette association ne puisse être interprétée comme une preuve de causalité directe.3,7
Références
- Calabrese EJ, Dhawan G, Kapoor R, Iavicoli I, Calabrese V. Qu'est-ce que l'hormèse et quelle est sa pertinence pour un vieillissement sain et la longévité ? Biogérontologie. Décembre 2015 ; 16(6) : 693-707. doi : 10.1007/s10522-015-9601-0. Voir sur PubMed ↗
- Sramek P, Simeckova M, Jansky L, Savlikova J, Vybiral S. Réponses physiologiques humaines à l'immersion dans de l'eau à différentes températures. Eur J Appl Physiol. Mars 2000 ; 81(5) : 436-442. doi : 10.1007/s004210050065. Voir sur PubMed ↗
- Laukkanen T, Khan H, Zaccardi F, Laukkanen JA. Association entre les bains de sauna et les événements cardiovasculaires mortels et la mortalité toutes causes confondues. JAMA Intern Med. Avril 2015 ; 175(4) : 542-548. doi : 10.1001/jamainternmed.2014.8187. Voir sur PubMed ↗
- Gibala MJ, McGee SL, Garnham AP, Howlett KF, Snow RJ, Hargreaves M. Un exercice intense de courte durée active les voies de signalisation AMPK et p38 MAPK et augmente l'expression de PGC-1alpha dans le muscle squelettique humain. J Appl Physiol. Mars 2009 ; 106(3) : 929-934. doi : 10.1152/japplphysiol.90880.2008. Voir sur PubMed ↗
- de Cabo R, Mattson MP. Effets du jeûne intermittent sur la santé, le vieillissement et les maladies. N Engl J Med. 26 décembre 2019 ; 381(26) : 2541-2551. doi : 10.1056/NEJMra1905136. Voir sur PubMed ↗
- Mattson MP, Longo VD, Harvie M. Impact du jeûne intermittent sur la santé et les processus pathologiques. Ageing Res Rev. Octobre 2017 ; 39 : 46-58. doi : 10.1016/j.arr.2016.10.005. Voir sur PubMed ↗
- Laukkanen T, Kunutsor SK, Khan H, Willeit P, Zaccardi F, Laukkanen JA. La pratique du sauna est associée à une réduction de la mortalité cardiovasculaire et améliore la prédiction des risques chez les hommes et les femmes : une étude de cohorte prospective. BMC Med. 29 novembre 2018 ; 16(1) : 219. doi : 10.1186/s12916-018-1198-0. Voir sur PubMed ↗
- Calabrese V, Cornelius C, Cuzzocrea S, Iavicoli I, Rizzarelli E, Calabrese EJ. Hormesis, cellular stress response and vitagenes as critical determinants in aging and longevity. Mol Aspects Med. Août 2011 ; 32(4-6) : 279-304. doi : 10.1016/j.mam.2011.10.007. Voir sur PubMed ↗