La hormesis es un fenómeno biológico en el que la exposición breve y en dosis bajas a un factor de estrés desencadena respuestas adaptativas que fortalecen el organismo. La exposición al frío, la sauna, el ayuno y el ejercicio activan las vías horméticas, incluyendo la liberación de norepinefrina, la inducción de proteínas de choque térmico, la activación de AMPK y la señalización de sirtuinas. El factor crítico es la relación dosis-respuesta: una dosis demasiado baja no produce ningún efecto, la dosis adecuada genera adaptación y una dosis excesiva causa daño.
Puntos clave
- La hormesis sigue una curva dosis-respuesta en forma de U invertida: un pequeño factor de estrés estimula una adaptación beneficiosa, mientras que una exposición excesiva produce daños.1
- La inmersión en agua fría activa el sistema nervioso simpático, y los estudios en humanos indican que la norepinefrina plasmática aumenta más del 500 % en comparación con los niveles en reposo.2
- En una cohorte prospectiva finlandesa de más de 2000 hombres, el uso más frecuente de la sauna se asoció con un riesgo sustancialmente menor de eventos cardiovasculares mortales en comparación con el uso una vez por semana.3
- Una sesión intensa de ejercicio intervalado de alta intensidad en humanos activa la AMPK y la p38 MAPK en el músculo esquelético y aumenta la expresión de PGC-1alfa, lo que indica la biogénesis mitocondrial.4
- El ayuno intermitente activa la autofagia a través de la señalización AMPK-mTOR y aumenta la actividad de la sirtuina, dos vías asociadas con el mantenimiento celular y la longevidad.5
- La relación dosis-respuesta hormética está muy conservada en todos los sistemas biológicos y es relevante para comprender los límites de la plasticidad adaptativa en los seres humanos.8
Capítulo 1: El concepto de hormesis: cómo el estrés se convierte en fuerza
La frase «lo que no te mata te hace más fuerte» es más que un proverbio. Refleja un mecanismo biológico específico que los investigadores han estudiado durante más de un siglo bajo el término hormesis.
La hormesis describe una relación bifásica entre la dosis y la respuesta en la que una dosis baja de un factor de estrés produce un efecto estimulante o beneficioso, mientras que una dosis alta del mismo factor de estrés produce un efecto inhibidor o perjudicial.1 Cuando se representa gráficamente, se obtiene la característica curva en forma de U invertida: una zona de dosis bajas en la que mejora el rendimiento biológico, un pico y una zona de dosis altas en la que el rendimiento disminuye o se acumulan los daños.
El concepto tiene sus raíces en la obra del médico del siglo XVI Paracelso, quien señaló que la diferencia entre un medicamento y un veneno suele ser la dosis. El marco científico moderno de la hormesis se desarrolló sustancialmente gracias al trabajo de toxicólogos y biogerontólogos a finales del siglo XX, quienes reconocieron que el fenómeno no era una excepción, sino una regla en todos los sistemas biológicos.1
Lo que hace que la hormesis sea especialmente relevante para la longevidad es la observación de que muchas de las respuestas adaptativas desencadenadas por factores de estrés leves —la producción de proteínas de choque térmico, la activación de enzimas reparadoras, la estimulación de la autofagia— son los mismos procesos que disminuyen con el envejecimiento. Los investigadores han propuesto que la capacidad de generar una respuesta hormética robusta puede definir por sí misma los límites de la plasticidad biológica y, en última instancia, la longevidad.8
Hay cuatro factores de estrés prácticos que revisten especial importancia para las personas interesadas en la longevidad: la exposición deliberada al frío, la exposición deliberada al calor, el ejercicio y el ayuno periódico. Cada uno de ellos activa vías horméticas superpuestas pero distintas, y la base empírica de cada uno de ellos en los seres humanos es cada vez mayor.
Capítulo 2: Hormesis por frío: norepinefrina, grasa parda y adaptación celular
La inmersión en agua fría y las duchas frías representan algunas de las prácticas horméticas deliberadas más antiguas de la historia. Desde un punto de vista fisiológico, la exposición breve al frío es un factor de estrés controlado que activa el sistema nervioso simpático, induciendo una cascada de respuestas adaptativas.
La respuesta más inmediata y bien documentada es un fuerte aumento de la norepinefrina plasmática. En un estudio controlado con hombres sanos sumergidos en agua a 14 grados centígrados, los investigadores informaron de un aumento de las concentraciones plasmáticas de noradrenalina de aproximadamente un 530 % en comparación con los niveles en reposo, con un aumento de la dopamina de aproximadamente un 250 %.2 Se entiende que esta activación simpática es uno de los principales factores que provocan los efectos agudos del resfriado sobre el estado de alerta y el estado de ánimo.
Más allá de la respuesta neuroquímica inmediata, la exposición repetida al frío se asocia con cambios adaptativos en la forma en que el cuerpo regula la temperatura y la tasa metabólica. Se sabe que el tejido adiposo marrón, un depósito de grasa especializado que genera calor quemando calorías, se activa con el frío y aumenta de volumen con la exposición repetida al frío en los seres humanos. La activación de este tejido representa una auténtica adaptación metabólica, no solo una respuesta aguda a la incomodidad.
A nivel celular, se ha estudiado la exposición al frío por su asociación con la expresión de proteínas inducibles por el frío y elementos de respuesta al estrés. El punto central desde la perspectiva de la hormesis es la dependencia de la dosis: se cree que las exposiciones breves y repetidas a una intensidad que genera una respuesta al estrés significativa pero tolerable son más beneficiosas que la exposición mínima o el frío extremo prolongado. El objetivo es el estímulo adaptativo, no la dosis máxima soportable.
Desde un punto de vista práctico, los protocolos de inmersión en agua fría estudiados en entornos de investigación suelen implicar temperaturas del agua entre 10 y 20 grados centígrados y duraciones de uno a diez minutos. La variación individual en la tolerancia al frío es considerable, y cualquier persona que considere exponerse deliberadamente al frío debe hacerlo de forma gradual y siendo consciente de las contraindicaciones, incluidas las afecciones cardiovasculares.
Capítulo 3: Hormesis térmica: proteínas de choque térmico y adaptación cardiovascular
La exposición al calor, en particular a través del uso tradicional de la sauna, es una de las prácticas horméticas más estudiadas en los seres humanos. Los datos de la cohorte finlandesa, en particular, han proporcionado algunas de las pruebas observacionales más convincentes que relacionan un factor de estrés térmico deliberado con resultados asociados a la longevidad.
En un estudio prospectivo de cohorte de 2315 hombres finlandeses de mediana edad a los que se hizo un seguimiento de hasta 20 años, Laukkanen y sus colegas examinaron la relación entre la frecuencia de los baños de sauna y la mortalidad. En comparación con los hombres que utilizaban la sauna una vez a la semana, los que la utilizaban entre cuatro y siete veces a la semana mostraban tasas sustancialmente más bajas de eventos cardiovasculares mortales y mortalidad por todas las causas, con asociaciones que persistían después de ajustar los factores de riesgo cardiovasculares convencionales, la actividad física y el estatus socioeconómico.3 Estos hallazgos se ampliaron posteriormente a las mujeres en un análisis independiente, en el que se observaron asociaciones direccionales similares.7
Hay que tener en cuenta algunas advertencias importantes sobre estos resultados. Los estudios observacionales de cohortes no pueden establecer una relación causal, y no se pueden descartar por completo los factores de confusión, como los hábitos saludables que se dan al mismo tiempo que el uso regular de la sauna. Los datos existentes representan asociaciones, más que beneficios causales probados.
El mecanismo biológico propuesto a través del cual la exposición al calor puede producir beneficios adaptativos se centra en las proteínas de choque térmico, en particular HSP70 y HSP90. Estas chaperonas moleculares son inducidas por el estrés celular de las temperaturas elevadas y desempeñan un papel en la protección de las proteínas contra el plegamiento incorrecto, facilitando la reparación celular y apoyando la regulación inmunológica. La inducción de proteínas de choque térmico representa una respuesta hormética: el estrés térmico leve de una sesión de sauna es suficiente para estimular la expresión de proteínas protectoras sin causar daño tisular.
Otras respuestas fisiológicas a la exposición al calor que se han documentado en estudios en humanos incluyen aumentos transitorios de la frecuencia cardíaca, mejoras en la distensibilidad arterial y expansión del volumen plasmático. Estas adaptaciones cardiovasculares se asemejan, en algunos aspectos, a los efectos del ejercicio aeróbico moderado, lo que ha llevado a los investigadores a describir el uso de la sauna como una forma de acondicionamiento cardiovascular pasivo.
Las temperaturas de las saunas en la tradición finlandesa suelen oscilar entre 80 y 100 grados centígrados con baja humedad, y las sesiones duran entre 10 y 20 minutos. Al igual que con la exposición al frío, la respuesta individual varía, y la exposición al calor está contraindicada en determinadas poblaciones clínicas. Cualquier persona con enfermedades cardiovasculares u otras afecciones de salud importantes debe consultar a un profesional sanitario cualificado antes de comenzar a practicar la sauna de forma habitual.
Capítulo 4: Hormesis del ejercicio: del estrés mitocondrial a la activación de la AMPK
El ejercicio es quizás el factor de estrés hormético más estudiado. Cada sesión de esfuerzo físico impone un estrés controlado al cuerpo —elevando las especies reactivas de oxígeno, agotando las reservas de glucógeno, generando subproductos metabólicos— y el cuerpo responde desarrollando capacidad de adaptación. El resultado, con el tiempo, es un organismo más fuerte y metabólicamente más eficiente.
A nivel celular, el ejercicio activa dos de las proteínas de señalización más importantes en la ciencia de la longevidad: AMPK (proteína quinasa activada por AMP) y PGC-1alfa (coactivador 1-alfa del receptor gamma activado por proliferadores de peroxisomas).
En un estudio de biopsia muscular humana, Gibala y sus colegas descubrieron que una sesión aguda de ejercicio intervalado de alta intensidad elevaba significativamente la fosforilación de la AMPK y la activación de la p38 MAPK en el músculo vasto lateral humano, con un aumento del ARNm de PGC-1alfa de aproximadamente el doble por encima de los niveles de reposo durante la recuperación.4 Esta firma molecular está asociada con el inicio de la biogénesis mitocondrial, el proceso mediante el cual las células construyen nuevas mitocondrias para aumentar su capacidad de producción de energía.
La AMPK funciona como un sensor de energía celular. Cuando la proporción de AMP con respecto al ATP aumenta, como ocurre durante el ejercicio intenso, el ayuno o los periodos de estrés energético, la AMPK se activa. Una vez activa, la AMPK promueve los procesos catabólicos (absorción de glucosa, oxidación de grasas, biogénesis mitocondrial) e inhibe los procesos anabólicos (crecimiento celular, síntesis de proteínas a través de mTOR). Este cambio metabólico es uno de los mecanismos centrales que vinculan el ejercicio con el mantenimiento celular asociado a la longevidad.
Dos modalidades de ejercicio parecen activar vías horméticas parcialmente distintas. El entrenamiento en la zona 2, caracterizado por un esfuerzo constante a una intensidad baja o moderada, se asocia con una activación sostenida de la AMPK y una biogénesis mitocondrial robusta a lo largo del tiempo. El entrenamiento por intervalos de alta intensidad produce una activación más aguda y pronunciada de la AMPK y la p38 MAPK por unidad de tiempo, junto con la liberación de miocinas, moléculas de señalización secretadas por la contracción muscular que influyen en otros tejidos, como el cerebro, el hígado y el tejido adiposo. Un programa de ejercicio bien diseñado con fines de longevidad puede beneficiarse de la incorporación de ambas modalidades.
El principio de hormesis se aplica claramente aquí: muy poco ejercicio no produce un estímulo adaptativo significativo, la dosis adecuada produce adaptación y el entrenamiento excesivo sin una recuperación adecuada conduce al síndrome de sobreentrenamiento, la supresión inmunológica y un mayor riesgo de lesiones. La recuperación no es la ausencia de entrenamiento, sino el momento en que se consolida la respuesta adaptativa.
Capítulo 5: Hormesis del ayuno: autofagia, activación de sirtuinas y limpieza celular
El ayuno periódico es uno de los factores de estrés hormético más potentes a disposición de los seres humanos. Cuando el cuerpo se ve privado de aporte calórico durante un periodo de tiempo suficiente, responde activando una serie de vías de supervivencia que dan prioridad al mantenimiento y la reparación celular por encima del crecimiento y la reproducción.
Dos de los eventos moleculares más importantes desencadenados por el ayuno son la inducción de la autofagia y la activación de la sirtuina.
La autofagia, del griego «autoconsumo», es el proceso celular mediante el cual se descomponen y reciclan las proteínas dañadas, los orgánulos disfuncionales y otros residuos celulares. Representa un mecanismo de control de calidad esencial para la longevidad celular y que se ve afectado por el envejecimiento. El ayuno activa la autofagia a través del eje AMPK-mTOR: a medida que disminuye la disponibilidad calórica, se activa la AMPK y se inhibe la mTOR (diana mecánica de la rapamicina). Dado que la mTOR normalmente suprime la autofagia, su inhibición permite que el programa de autofagia continúe.5
Las sirtuinas son una familia de enzimas desacetilasas que regulan una amplia gama de procesos biológicos, entre los que se incluyen la reparación del ADN, la inflamación y la adaptación metabólica. La actividad de las sirtuinas depende de la disponibilidad de NAD+, cuyos niveles aumentan durante el ayuno a medida que la célula se inclina hacia la oxidación de los ácidos grasos. De esta manera, el ayuno vincula directamente el estado energético de la célula con su capacidad de mantenimiento y reparación.6
Una revisión exhaustiva realizada por de Cabo y Mattson en la revista New England Journal of Medicine resumió las pruebas que sugieren que el ayuno intermitente, incluidos los protocolos de alimentación con restricción de tiempo y ayuno en días alternos, activa estas vías adaptativas conservadas en los seres humanos y se asocia con una serie de mejoras metabólicas, entre las que se incluyen una mayor sensibilidad a la insulina, una reducción de los marcadores inflamatorios y una mayor resistencia al estrés.5 Sin embargo, los revisores señalaron que traducir los resultados de modelos animales y ensayos clínicos a corto plazo en recomendaciones clínicas definitivas a largo plazo requiere más estudios.
El principio de hormesis se aplica al ayuno al igual que a todos los factores estresantes. Los períodos de ayuno ocasionales de 12 a 24 horas son coherentes con los patrones bajo los cuales evolucionaron los seres humanos y son bien tolerados por la mayoría de los adultos sanos. El ayuno prolongado más allá de este rango implica un perfil de riesgo diferente y queda fuera del alcance de esta descripción general educativa. Las personas con antecedentes de trastornos alimentarios, diabetes u otras afecciones de salud relevantes no deben seguir protocolos de ayuno sin supervisión médica.
Capítulo 6: El principio de dosis-respuesta: cómo falla la hormesis cuando la dosis es incorrecta
La comprensión de la hormesis no está completa sin comprender dónde se rompe. La curva en forma de U invertida significa que la misma intervención que es beneficiosa en una dosis moderada puede ser neutra en una dosis baja y perjudicial en una dosis alta.
En el contexto del ejercicio, este modo de fallo es el síndrome de sobreentrenamiento, un estado en el que el estrés acumulado por el ejercicio sin una recuperación adecuada suprime la función inmunitaria, aumenta el riesgo de lesiones, eleva el cortisol en reposo y puede acelerar, en lugar de ralentizar, los marcadores del envejecimiento biológico. La respuesta adaptativa solo se produce durante el periodo de recuperación, no durante el estrés en sí.
En el contexto del calor y el frío, los modos de fallo son la hipertermia y la hipotermia, respectivamente, extremos que causan daños fisiológicos en lugar de adaptación.
En el contexto del ayuno, una restricción calórica severa prolongada puede provocar pérdida muscular, alteraciones hormonales y deficiencias nutricionales cuando se lleva a cabo sin la supervisión adecuada.
Un hallazgo de la investigación sobre la hormesis que tiene relevancia directa para el uso de suplementos es la paradoja antioxidante. Algunos estudios han demostrado que la suplementación con altas dosis de antioxidantes inmediatamente después del ejercicio atenúa la señalización adaptativa asociada al ejercicio, posiblemente porque las especies reactivas de oxígeno producidas durante el ejercicio sirven como señal hormética inicial para la activación de la AMPK y la biogénesis mitocondrial. Esto no significa que los antioxidantes sean perjudiciales, ya que son beneficiosos en contextos adecuados, pero ilustra que las respuestas adaptativas del cuerpo al estrés están finamente calibradas y pueden verse alteradas si se satura la señal.
El principio práctico de la investigación sobre la hormesis es el siguiente: buscar la dosis que produzca una respuesta al estrés significativa pero recuperable, permitir una recuperación adecuada y repetir. La consistencia y la dosificación adecuada producen adaptación. La intensidad extrema sin recuperación no lo hace.
Capítulo 7: Suplementos que interactúan con las vías horméticas
Se han estudiado varios suplementos por su potencial para apoyar las vías celulares activadas por factores de estrés horméticos. Esta sección los presenta únicamente en un contexto educativo. Ninguna afirmación sobre los suplementos que se hace aquí va más allá de lo que actualmente respaldan las pruebas en humanos y los marcos normativos.
El magnesio interviene en más de 300 reacciones enzimáticas y desempeña un papel en el metabolismo energético, la función muscular y la síntesis de proteínas. El magnesio contribuye al metabolismo energético normal y ayuda a reducir el cansancio y la fatiga, dos declaraciones de propiedades saludables aprobadas por la EFSA relevantes para la recuperación del estrés provocado por el ejercicio. La suplementación con magnesio para mantener los niveles adecuados, especialmente en personas con una gran carga de ejercicio, es una estrategia nutricional razonable.
La creatina aumenta el rendimiento físico en series sucesivas de ejercicios de corta duración y alta intensidad, y mejora la fuerza muscular en adultos mayores de 55 años que realizan entrenamiento de resistencia regular, ambas afirmaciones aprobadas por la EFSA. Esto hace que la creatina sea directamente relevante para la hormesis del ejercicio, ya que respalda las exigencias de rendimiento agudo del entrenamiento por intervalos de alta intensidad y los ejercicios de resistencia.
El resveratrol y los polifenoles relacionados se han estudiado como posibles compuestos xenohorméticos, moléculas dietéticas que pueden activar algunas de las mismas vías de respuesta al estrés que los factores de estrés físico, incluida la activación de la sirtuina. Las pruebas en humanos de estos efectos siguen siendo preliminares y requieren una interpretación cautelosa.
El NMN y el NR, como precursores del NAD+, se estudian por su potencial para apoyar las funciones dependientes del NAD+ de las sirtuinas, que se activan mediante la hormesis del ayuno. Se están realizando ensayos en humanos y no deben hacerse afirmaciones sobre resultados específicos más allá de lo que respaldan las pruebas actuales.
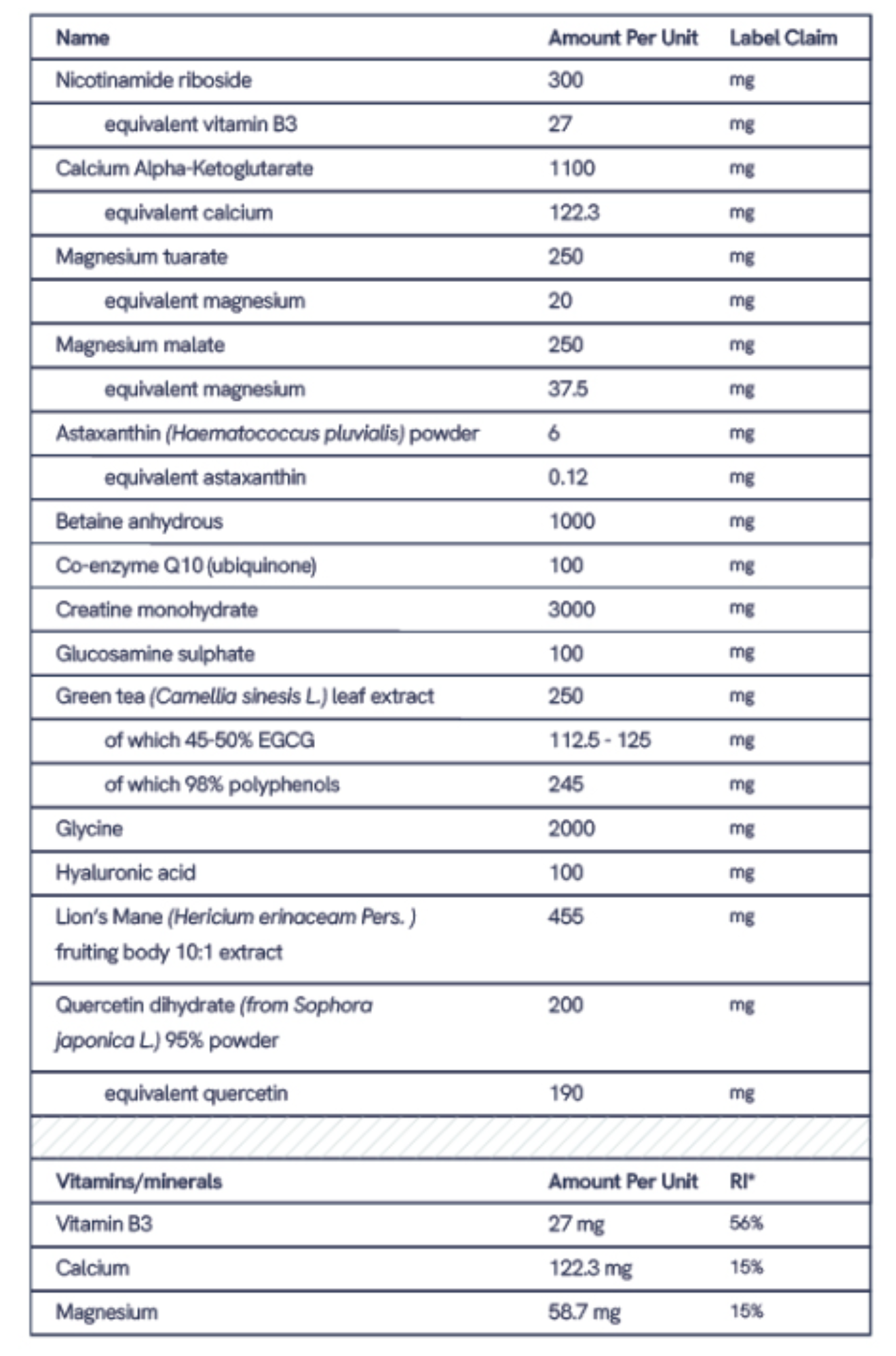
Longevity Complete de The Longevity Store está formulado para incluir magnesio, creatina, vitaminas B, vitamina C, zinc y otros nutrientes basados en la evidencia. Ha sido probado de forma independiente en el laboratorio Eurofins y cuenta con la certificación NZVT de ausencia de dopaje. Cuando es relevante para apoyar el metabolismo energético normal, la función muscular y la recuperación, sus ingredientes se formulan en dosis investigadas.
Preguntas y respuestas
¿Qué significa realmente la palabra «hormesis»?
Hormesis proviene de la palabra griega que significa «poner en marcha» o «estimular». En biología, describe un fenómeno de dosis-respuesta en el que una dosis baja de un factor de estrés produce un efecto estimulante beneficioso y una dosis alta del mismo factor de estrés produce un efecto inhibidor o perjudicial.1 Es la base científica de la observación de que pequeñas cantidades de estrés físico o fisiológico pueden fortalecer, en lugar de debilitar, los sistemas biológicos.
¿Por qué la exposición al frío parece mejorar el estado de ánimo y la energía?
La inmersión en agua fría activa el sistema nervioso simpático, lo que produce una notable liberación de norepinefrina. Estudios en humanos han documentado aumentos de norepinefrina en plasma de más del 500 % durante la inmersión en frío en comparación con los niveles en reposo.2 La norepinefrina está asociada con el estado de alerta, la atención y el afecto positivo. Esta respuesta neuroquímica aguda es uno de los posibles factores que contribuyen a la mejora del estado de ánimo y la energía que muchas personas reportan después de la exposición al frío.
¿Existen pruebas científicas sobre la sauna y la longevidad?
Sí, aunque las pruebas son observacionales y no proceden de ensayos controlados aleatorios. Un estudio prospectivo de cohortes finlandés descubrió que los hombres que utilizaban la sauna entre cuatro y siete veces por semana tenían tasas sustancialmente más bajas de eventos cardiovasculares mortales en comparación con los que la utilizaban una vez por semana, después de ajustar los factores de riesgo cardiovascular conocidos.3 Investigaciones posteriores ampliaron estos hallazgos a las mujeres.7 Estos estudios no pueden demostrar la causalidad, pero los datos son coherentes y el mecanismo biológico (inducción de proteínas de choque térmico y acondicionamiento cardiovascular) es plausible.
¿Qué ocurre en las células musculares durante el ejercicio a nivel molecular?
Durante el ejercicio intenso, la demanda energética de los músculos en contracción provoca un aumento de la relación AMP/ATP. Esto activa la AMPK, que a su vez estimula la PGC-1 alfa, un regulador maestro de la biogénesis mitocondrial. Los estudios de biopsias musculares humanas han confirmado que incluso una breve sesión de ejercicio intervalado de alta intensidad es suficiente para activar la AMPK y la señalización p38 MAPK y aumentar la expresión del gen PGC-1 alfa en cuestión de horas.4 Tras repetidas sesiones, esto conduce a un aumento de la densidad mitocondrial y la capacidad aeróbica.
¿Cómo desencadena el ayuno la autofagia?
Durante el ayuno, el agotamiento de la glucosa y los aminoácidos reduce la actividad de mTOR, el sensor de crecimiento celular que normalmente suprime la autofagia. Simultáneamente, la AMPK se activa por la caída del ATP celular. Estos dos cambios juntos liberan el programa de autofagia, lo que permite a las células descomponer y reciclar las proteínas y orgánulos dañados. Se cree que este proceso es un importante mecanismo de mantenimiento celular que disminuye con el envejecimiento.5
¿Los cuatro factores de estrés hormético (frío, calor, ejercicio y ayuno) funcionan a través de las mismas vías?
Comparten algunos nodos de señalización comunes, en particular la activación de AMPK, pero cada factor de estrés también activa vías distintas. El frío afecta principalmente al sistema nervioso simpático y a las proteínas de choque frío. El calor induce principalmente proteínas de choque térmico y adaptaciones cardiovasculares. El ejercicio activa AMPK, p38 MAPK y la secreción de miocinas. El ayuno activa la señalización AMPK-mTOR, la actividad de las sirtuinas y la producción de cuerpos cetónicos. El solapamiento sugiere que es posible una sinergia cuando los factores estresantes se combinan de forma inteligente con una recuperación adecuada, aunque las pruebas formales de los protocolos de combinación óptimos en humanos siguen siendo limitadas.6
¿Se puede abusar de la hormesis?
Sí. La relación dosis-respuesta en forma de U invertida significa que todos los factores de estrés horméticos tienen un límite superior más allá del cual se vuelven perjudiciales. El síndrome de sobreentrenamiento, la hipertermia, la hipotermia y la restricción calórica severa representan los modos de fallo cuando los factores de estrés horméticos se aplican con una intensidad excesiva o sin una recuperación adecuada. El objetivo es identificar la dosis que produce una respuesta adaptativa significativa, no la dosis máxima tolerable.1
¿Debo tomar suplementos antioxidantes los días que hago ejercicio?
Se trata de un ámbito en el que las pruebas sugieren que hay que actuar con cautela en cuanto al momento de administración. Algunas investigaciones indican que los suplementos antioxidantes en dosis elevadas tomados inmediatamente después del ejercicio pueden atenuar las especies reactivas de oxígeno que sirven como señal hormética inicial para la activación de la AMPK y la adaptación mitocondrial. Esto no significa que los nutrientes antioxidantes sean perjudiciales en general —el zinc, la vitamina C y el selenio desempeñan un papel importante en la protección celular normal—, pero el momento de administración en relación con el ejercicio puede ser importante. Es aconsejable consultar a un profesional sanitario cualificado sobre su protocolo específico de suplementos.
Preguntas frecuentes
¿Qué es la hormesis en términos sencillos?
La hormesis es el principio biológico según el cual pequeñas dosis de un factor de estrés pueden fortalecer el cuerpo. El agua fría, el calor, el ejercicio y el ayuno son ejemplos prácticos: cada uno de ellos crea un estrés controlado que hace que el cuerpo se adapte y se vuelva más resistente con el tiempo. La clave está en la dosis: una dosis demasiado pequeña no produce ningún beneficio, la cantidad adecuada produce adaptación y una dosis excesiva causa daño.1
¿La hormesis es lo mismo que el estrés?
La hormesis es un tipo específico de respuesta beneficiosa al estrés. No todo el estrés es hormético; por ejemplo, el estrés psicológico crónico no produce los mismos beneficios adaptativos que los estresantes físicos breves. El estrés hormético se caracteriza por su breve duración, intensidad controlada y tiempo de recuperación adecuado, lo que permite al cuerpo generar una respuesta adaptativa en lugar de agotarse crónicamente.
¿Cómo se relaciona la hormesis por ejercicio con la longevidad?
El ejercicio activa la AMPK y la PGC-1 alfa en el músculo esquelético humano, lo que impulsa la biogénesis mitocondrial y mejora la eficiencia metabólica.4 Estas adaptaciones están asociadas con una mejora de los indicadores de salud, como la capacidad aeróbica, la sensibilidad a la insulina y el equilibrio inflamatorio. El principio hormético explica por qué el ejercicio de intensidad moderada realizado de forma constante es más beneficioso para la longevidad que la ausencia de ejercicio o el entrenamiento extremo sin recuperación.
¿Puede el ayuno intermitente favorecer la hormesis?
Sí. El ayuno periódico activa la vía AMPK-mTOR, estimulando la autofagia y la actividad de las sirtuinas, procesos de mantenimiento celular asociados a la investigación sobre la longevidad. Una revisión publicada en la revista New England Journal of Medicine concluyó que el ayuno intermitente activa estas vías en los seres humanos y está asociado a mejoras metabólicas, aunque los autores señalaron que las recomendaciones clínicas a largo plazo requieren más estudios.5
¿El uso de la sauna es una forma de hormesis?
El uso de la sauna se considera una práctica de hormesis térmica. Induce la expresión de proteínas de choque térmico, la adaptación cardiovascular y respuestas inflamatorias transitorias en los seres humanos. Los datos de cohortes observacionales de Finlandia asocian el uso regular de la sauna con una menor mortalidad cardiovascular, aunque esta asociación no puede interpretarse como prueba de causalidad directa.3,7
Referencias
- Calabrese EJ, Dhawan G, Kapoor R, Iavicoli I, Calabrese V. ¿Qué es la hormesis y cuál es su relevancia para el envejecimiento saludable y la longevidad? Biogerontología. Diciembre de 2015; 16(6):693-707. doi: 10.1007/s10522-015-9601-0. Ver en PubMed ↗
- Sramek P, Simeckova M, Jansky L, Savlikova J, Vybiral S. Respuestas fisiológicas humanas a la inmersión en agua a diferentes temperaturas. Eur J Appl Physiol. Marzo de 2000; 81(5):436-442. doi: 10.1007/s004210050065. Ver en PubMed ↗
- Laukkanen T, Khan H, Zaccardi F, Laukkanen JA. Asociación entre los baños de sauna y los eventos cardiovasculares mortales y la mortalidad por todas las causas. JAMA Intern Med. Abril de 2015; 175(4):542-548. doi: 10.1001/jamainternmed.2014.8187. Ver en PubMed ↗
- Gibala MJ, McGee SL, Garnham AP, Howlett KF, Snow RJ, Hargreaves M. El ejercicio breve e intenso por intervalos activa la señalización AMPK y p38 MAPK y aumenta la expresión de PGC-1alfa en el músculo esquelético humano. J Appl Physiol. Marzo de 2009; 106(3):929-934. doi: 10.1152/japplphysiol.90880.2008. Ver en PubMed ↗
- de Cabo R, Mattson MP. Efectos del ayuno intermitente sobre la salud, el envejecimiento y las enfermedades. N Engl J Med. 26 de diciembre de 2019; 381(26):2541-2551. doi: 10.1056/NEJMra1905136. Ver en PubMed ↗
- Mattson MP, Longo VD, Harvie M. Impacto del ayuno intermitente en la salud y los procesos patológicos. Ageing Res Rev. Octubre de 2017; 39:46-58. doi: 10.1016/j.arr.2016.10.005. Ver en PubMed ↗
- Laukkanen T, Kunutsor SK, Khan H, Willeit P, Zaccardi F, Laukkanen JA. El baño de sauna se asocia con una reducción de la mortalidad cardiovascular y mejora la predicción del riesgo en hombres y mujeres: un estudio prospectivo de cohortes. BMC Med. 29 de noviembre de 2018; 16(1):219. doi: 10.1186/s12916-018-1198-0. Ver en PubMed ↗
- Calabrese V, Cornelius C, Cuzzocrea S, Iavicoli I, Rizzarelli E, Calabrese EJ. Hormesis, respuesta al estrés celular y vitagenes como determinantes críticos en el envejecimiento y la longevidad. Mol Aspects Med. Agosto de 2011; 32(4-6):279-304. doi: 10.1016/j.mam.2011.10.007. Ver en PubMed ↗